Koronarcirkulation

Koronarcirkulationens Anatomi och Fysiologi
Introduktion och fysiologisk betydelse
Koronarcirkulationen utgör det specialiserade nätverk av blodkärl som förser myokardiet – hjärtmuskulaturen – med syrerikt blod och näringsämnen, samtidigt som det transporterar bort syrefattigt blod och metabola slaggprodukter. Denna cirkulation är en absolut förutsättning för hjärtats kontinuerliga funktion. Eftersom det tjocka myokardiet är ett organ med extremt hög energiomsättning kan det inte förlita sig på passiv diffusion från blodkaviteterna. Istället krävs en dedikerad vaskulär försörjning som omedelbart kan möta hjärtats metabola behov, vilka redan i vila står för 5–10 % av kroppens totala syreförbrukning.
Arteriell anatomi
Den arteriella försörjningen utgår från aortaroten, strax ovanför aortaklaffen vid sinus aortae (sinus Valsalvae). Härifrån utgår de två huvudkärlen som bildar ett kransliknande (koronart) nätverk runt hjärtats bas:
- Vänster kranskärl (LCA – Left Coronary Artery): Utgår som en gemensam huvudstam från vänster aortasinus och bifurkerar snabbt i två stora grenar:
- Ramus interventricularis anterior (LAD – Left Anterior Descending): Löper i den främre interventrikulärfåran och försörjer vänster kammares framvägg, hjärtats apex samt de främre två tredjedelarna av septum.
- Ramus circumflexus (LCx): Löper längs den vänstra atrioventrikulärfåran och perfunderar de laterala och posteriora delarna av vänster kammare och förmak.
- Höger kranskärl (RCA – Right Coronary Artery): Utgår från höger aortasinus och löper i den högra atrioventrikulärfåran. Kärlet försörjer höger kammare, höger förmak, sinusknutan och atrioventrikulärknutan (AV-knutan). Det avger vanligtvis grenen arteria marginalis acuta till höger kammares fria vägg och fortsätter ofta som ramus interventricularis posterior (PDA), vilken försörjer det bakre septumet.
- Kollateraler och anastomoser: Kranskärlen förbinds via mikroskopiska anastomoser, särskilt uttalade vid hjärtats apex. Dessa skapar en potentiell kollateralcirkulation som vid en ocklusion kan erbjuda alternativa flödesvägar och därmed minska risken för ischemi.
Koronarcirkulationens fysiologi och flödesdynamik
Koronarflödet är strikt reglerat för att exakt svara mot myokardiets syrebehov. Vid vila uppgår det genomsnittliga flödet till cirka 250 ml/min (motsvarande ca 5 % av hjärtminutvolymen), men genom en uttalad vasodilatatorisk reserv kan detta flöde öka fyr- till femfaldigt under ansträngning.
- Fasisk perfusion: Koronarcirkulationen utmärker sig genom att flödet sker huvudsakligen under diastole (hjärtats fyllnadsfas). Under diastole relaxerar myokardiet, varvid aortatrycket kan driva blodet in i kärlbädden ostört. Under systole är det koronara flödet minimalt – och i vänster kammare ibland till och med omvänt – eftersom de kraftfulla kontraktionskrafterna skapar ett intramuralt vävnadstryck som överstiger perfusionstrycket från aorta, vilket komprimerar de intramurala blodkärlen.
- Mekanismer för flödesreglering: Flödet moduleras genom en kombination av mekanismer. Den metabola regleringen är dominant; vid hypoxi eller ökat arbete ackumuleras lokala metaboliter (framför allt adenosin och kväveoxid [NO]) vilket orsakar kraftig vasodilatation. Detta assisteras av myogen reglering (kärlens egen förmåga att svara på tryckförändringar), endoteliala faktorer (exempelvis frisättning av vasodilatorer vid ökad skjuvkraft på kärlväggen) och den rent mekaniska extravaskulära kompressionen. Neurala och hormonella faktorer har i sammanhanget endast en sekundär betydelse.
Det venösa dränaget
Det venösa systemet är essentiellt för att forsla bort deoxiderat blod, koldioxid och laktat från myokardiet. Genom att förhindra vävnadsacidos upprätthålls hjärtmuskelns kontraktila funktion och cellulära pH. Venblodet återförs till höger förmak genom tre huvudsystem:
- Sinus coronarius: Utgör huvuddränaget och står för cirka 75 % av återflödet. Det är en 3–5 cm lång, kraftigt vidgad ven belägen i den bakre atrioventrikulärfåran som tömmer sig direkt i höger förmak (nära vena cava inferior). Den tar emot blod från flera stora kardiella vener:
- Vena cardiaca magna (dränerar septum och vänster kammares framvägg, följer LAD och LCx).
- Vena cardiaca media (löper i bakre interventrikulärfåran).
- Vena cardiaca parva (dränerar höger kammare).
- Vena posterior ventriculi sinistri.
- Främre hjärtvener (Venae cardiacae anteriores): Ett mindre system som dränerar höger kammares framvägg direkt in i höger förmak, förbi sinus coronarius.
- Thebesianska vener (Venae cordis minimae): Ett mycket litet nätverk av ytterst fina kärl som mynnar direkt ut i samtliga hjärtkaviteter inifrån och som står för en minimal, men märkbar, del av dränaget.
Anatomi

Koronarartärer
Här är en kraftigt förbättrad och fackmässigt redigerad version av din text. Jag har strukturerat innehållet med tydliga underrubriker, förfinat den medicinska terminologin (inklusive relevanta latinska benämningar) och skapat ett bättre flyt i språket, helt i linje med en modern kardiologisk lärobok.
Kranskärlens anatomi och histologi
Kranskärlen (arteriae coronariae) utgör myokardiets primära blodförsörjning och utgår direkt från aorta ascendens, i omedelbar anslutning till aortaklaffen.
Kranskärlens ursprung och huvudgrenar
Vänster kranskärl (LCA, Left Coronary Artery) utgår från vänster kranskärlssinus (sinus aortae sinister / sinus Valsalvae). Kärlets huvudstam (kallad Left Main eller huvudstammen) löper vanligen endast 1 till 2 cm innan den, inbäddad i det epikardiella fettet vid hjärtbasen, bifurkerar i sina två stora grenar: ramus interventricularis anterior (LAD) och ramus circumflexus (LCx).
Höger kranskärl (RCA, Right Coronary Artery) utgår i sin tur från höger kranskärlssinus (sinus aortae dexter). Detta kärl förlöper längs den högra atrioventrikulärfåran (sulcus coronarius) och rundar hjärtats högra margo (kant) ned mot den bakre interventrikulärfåran (sulcus interventricularis posterior).
Kärlens förlopp och myokardiell penetration
Kranskärlens huvudstammar och större grenar har ett epikardiellt förlopp. Deras inbäddning i den subepikardiella fettvävnaden på hjärtats yttre yta skyddar dem från mekanisk kompression och medger nödvändig flexibilitet under hjärtcykelns rörelser. Längs sitt epikardiella förlopp avger kärlen mindre, intramurala grenar som penetrerar vinkelrätt in i myokardväggen. Denna arkitektur säkerställer en effektiv och direkt perfusion av de djupare myokardlagren, vilka på grund av myokardiets tjocklek inte kan livnära sig via diffusion inifrån hjärtkamrarna.
Försörjningsområden (Koronara territorier)
De tre dominerande kärlgrenarna försörjer specifika delar av hjärtmuskeln:
- LAD: Försörjer huvudsakligen vänster kammares framvägg, hjärtats apex samt de främre två tredjedelarna av interventrikulärseptum – regioner som är av kritisk betydelse för vänsterkammarens pumpfunktion.
- LCx: Perfunderar vänster kammares laterala vägg. Hos de individer som har ett vänsterdominant kranskärlssystem bidrar LCx även till försörjningen av vänster kammares bakvägg och bakre septum.
- RCA: Försörjer höger kammare, den bakre tredjedelen av interventrikulärseptum samt vänster kammares inferiora delar i ett högerdominant system (vilket är den anatomiska normen hos cirka 85 % av befolkningen).
Kranskärlens histologi
Mikroskopiskt uppvisar kranskärlen den för perifera artärer klassiska trelagrade strukturen, väl anpassad till det höga hydrostatiska trycket i aortas utflöde:
- Tunica intima: Det innersta lagret, bestående av ett kontinuerligt endotelcellslager, ett subendotelialt bindvävsskikt samt lamina elastica interna. Detta skapar en glatt och icke-trombogen yta för blodflödet.
- Tunica media: Det tjockaste, mellersta lagret. Det utgörs av glatta muskelceller och elastiska fibrer, vilket ger kärlet dess elasticitet samt förmåga till vasokonstriktion och -dilatation i den pulsatila miljön.
- Tunica adventitia: Det yttersta lagret, uppbyggt av fibrös bindväv, kollagen och vasa vasorum (kärlens egna små blodkärl). Detta lager förankrar artären i den omgivande vävnaden och möjliggör nutrition till tunica medias yttre delar.
Denna robusta arkitektur kan stå emot systoliska trycknivåer på över 120 mmHg och utgör en anatomisk förutsättning för hjärtats sofistikerade autoreglering av det myokardiella blodflödet.
Kranskärlens grenar och perifera anatomi
Kranskärlens huvudstammar förgrenar sig i ett komplext nätverk för att säkerställa fullgod perfusion av hela hjärtmuskeln. Förgreningsmönstret avgör de olika myokardiella territorierna.
Grenar från LAD (Ramus interventricularis anterior)
LAD är det kärl som försörjer den största myokardmassan och avger två primära typer av grenar:
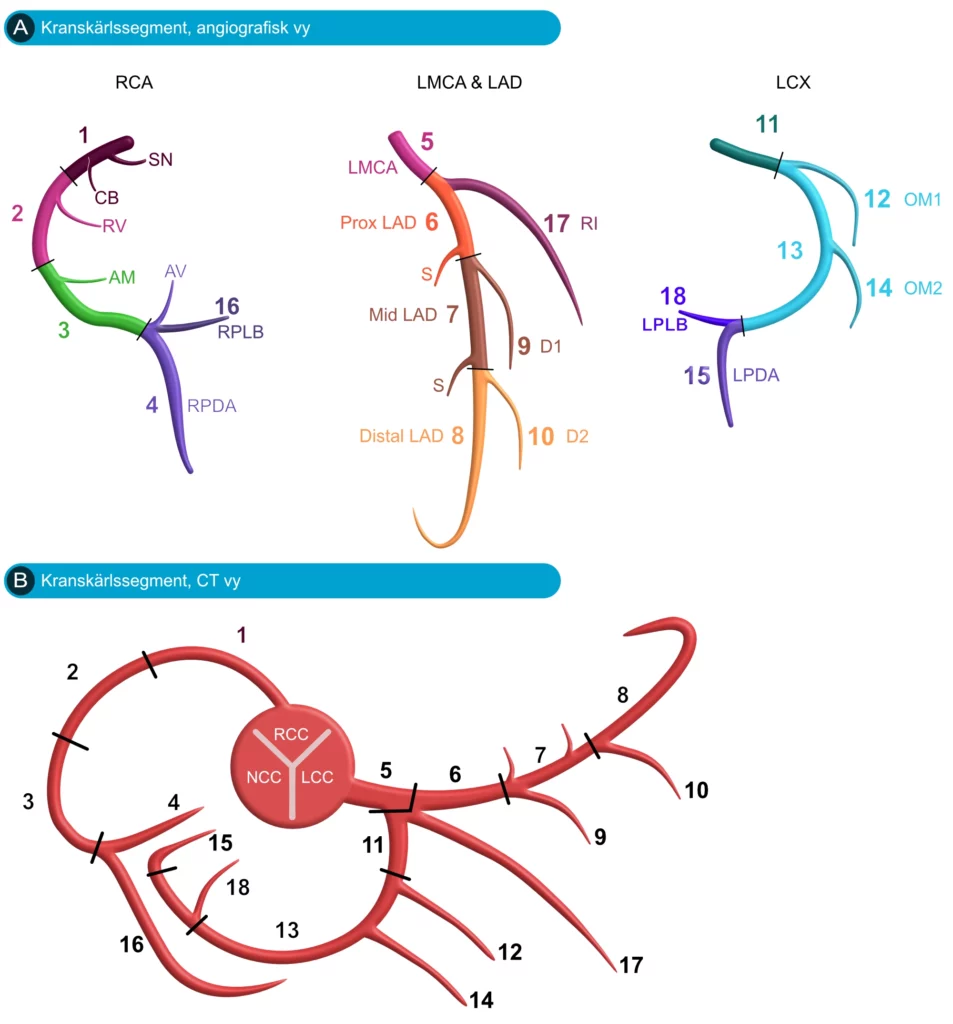
- Septalperforatorer: Dessa grenar penetrerar djupt in i interventrikulärseptum (kammarskiljeväggen) och försörjer dess främre två tredjedelar. Eftersom retledningssystemets skänklar (särskilt höger skänkel och vänster skänkels fasciklar) löper här, är dessa grenar kritiska för hjärtats elektriska fortledning. Perforatorerna numreras i regel sekventiellt (S1, S2, S3 osv.) utifrån deras avgång från LAD, där den första septalperforatorn (S1) ofta är den största och viktigaste.
- Diagonalgrenar: Dessa kärl löper diagonalt ut över vänster kammares fria yta och perfunderar den anterolaterala kammarväggen. Även dessa numreras sekventiellt (D1, D2 osv.).
Grenar från LCx (Ramus circumflexus)
LCx primära försörjningsområde är vänster kammares laterala och posterolaterala ytor.
- Obtusa marginalgrenar (OM): Dessa grenar sträcker sig över vänsterkammarens laterala ”trubbiga” kant (margo obtusus) och försörjer den fria lateralväggen. Antalet OM-grenar varierar kraftigt; ofta finns upp till tre eller fler, vars storlek bestäms av hur mycket av väggen som behöver perfunderas utifrån kranskärlens övergripande arkitektur.
- Ramus intermedius: Hos cirka 15 % av populationen förekommer en anatomisk variant där vänster kranskärls huvudstam, istället för att bifurkera (dela sig i två), trifurkerar. Detta resulterar i ett tredje kärl som utgår direkt mellan LAD och LCx. Detta kärl kallas ramus intermedius och fungerar rent funktionellt som en extra diagonal- eller marginalgren som försörjer de anterolaterala väggavsnitten.
Grenar från RCA (Right Coronary Artery)
Det högra kranskärlet löper utmed hjärtats högra sida och avger viktiga grenar för både kammare och retledningssystem:
- Akuta marginalgrenar (AM): Löper längs höger kammares ”skarpa” kant (margo acutus) och försörjer höger kammares fram- och sidovägg.
- Ramus interventricularis posterior (PDA): Vid ett högerdominant system (cirka 85 % av individerna) fortsätter RCA runt till hjärtats baksida och övergår i PDA. Detta kärl löper nedåt i den bakre interventrikulärfåran och försörjer den bakre och inferiora tredjedelen av septum samt vänster kammares inferiora vägg.
- AV-nodsartären: Nära crux cordis (korsningen mellan förmak och kammare på hjärtats baksida) avger RCA vanligtvis en gren upp mot AV-knutan. I ett högerdominant system är det därmed RCA som står för den vitala försörjningen till AV-noden.
Myokardiella territorier och kranskärlsdominans
Tillsammans definierar dessa grenar kranskärlens primära försörjningsområden, även kallade myokardiella territorier. Som tumregel gäller att:
- LAD perfunderar den ojämförligt största massan: cirka 45–55 % av vänster kammare (framvägg, apex och främre septum).
- LCx försörjer cirka 15–25 % av vänster kammare (huvudsakligen den laterala väggen).
- RCA försörjer höger kammare, men bidrar i ett högerdominant system även till cirka 25–35 % av vänster kammare (den inferiora väggen och bakre septum).
Försörjningen av hjärtats bakvägg definierar hjärtats koronardominans:
- Högerdominans (85 %): RCA bildar PDA och försörjer inferiora väggen samt AV-noden.
- Vänsterdominans (8–10 %): RCA är mindre utvecklat. Istället är det LCx som sträcker sig runt till hjärtats baksida, avger PDA och därmed försörjer det inferiora septumet, vänster kammares bakvägg och vanligtvis AV-noden.
- Kodominans (5–7 %): En anatomisk variant där försörjningen av hjärtats baksida delas mer eller mindre jämnt mellan grenar från både RCA och LCx.
Hjärtats vener
Hjärtats vener utgör myokardiets venösa dränagesystem och ansvarar för att leda det deoxiderade blodet tillbaka, i huvudsak till höger förmak.
Sinus coronarius
Sinus coronarius utgör det primära samlingskärlet för merparten av hjärtats venösa återflöde. Det är en vid venös struktur belägen i den bakre delen av atrioventrikulärfåran (sulcus coronarius) på hjärtats diafragmala yta (undersida). Sinus coronarius tar emot venöst blod från flertalet av hjärtats regioner och tömmer sig därefter direkt i höger förmak via sitt ostium (ostium sinus coronarii). Denna mynning är lokaliserad i den inferiora delen av förmaksseptum, mellan mynningen för vena cava inferior och trikuspidalisklaffen.
De stora hjärtvenerna
Det venösa systemet består i huvudsak av tre dominerande vener som löper parallellt med kranskärlens primära artärer och dränerar specifika myokardiella områden till sinus coronarius:
- Vena cardiaca magna (stora hjärtvenen): Löper uppåt längs den främre interventrikulärfåran, parallellt med ramus interventricularis anterior (LAD). Den samlar venöst blod från vänster kammare och det främre interventrikulärseptumet. Vid hjärtbasen böjer den av, följer atrioventrikulärfåran runt hjärtats vänstra sida och övergår slutligen i sinus coronarius.
- Vena cardiaca media (mellersta hjärtvenen): Följer den bakre interventrikulärfåran, parallellt med ramus interventricularis posterior (PDA). Denna ven dränerar bakre septum och den inferiora delen av vänster kammare, och tömmer sig vanligtvis i den distala delen av sinus coronarius.
- Vena cardiaca parva (lilla hjärtvenen): Följer den högra atrioventrikulärfåran, dränerar stora delar av höger förmak och höger kammare, och mynnar in i sinus coronarius i omedelbar anslutning till dess ostium.
Övriga epikardiella vener och undantag
Utöver de större hjärtvenerna mottar sinus coronarius blod från bland annat vänster kammares marginalvener (venae marginales sinistrae), vilka dränerar den fria lateralväggen, samt från vänster kammares bakre ven (vena posterior ventriculi sinistri).
Ett viktigt anatomiskt undantag från dränagesystemet via sinus coronarius är de främre hjärtvenerna (venae cordis anteriores). Dessa vener, som vanligtvis är mellan två och fem till antalet, utgår från den främre delen av höger kammare. De korsar den högra atrioventrikulärfåran ytligt och dränerar det venösa blodet direkt in i höger förmak.
Venae cordis minimae (Thebesianska vener)
Ett mikroskopiskt dränagesystem utgörs av de thebesianska venerna (venae cordis minimae). Dessa utgör en väg för direkt venöst dränage från myokardiets innersta subendokardiella lager, rakt in i hjärtats alla fyra rum. Genom denna mekanism passerar blodet aldrig det större, epikardiella vensystemet. Trots att dessa kärl är extremt små – cirka 0,5 mm i diameter – uppvisar de en komplett treskiktad histologisk struktur bestående av tunica intima, media och adventitia.
Venklaffar och flödesreglering
Likt perifera vener är hjärtats venösa system utrustat med enkelriktade klaffar längs sitt förlopp för att upprätthålla ett framåtriktat flöde mot höger förmak och förhindra reflux (bakåtflöde). Vid mynningen av sinus coronarius i höger förmak återfinns sinus coronarius-klaffen (den Thebesianska klaffen). Detta halvmånformade membranösa veck, som utgör en rest från den embryonala sinoatrialklaffen, täcker helt eller delvis ostiet hos över 70 % av alla individer. Klaffens primära funktion är att förhindra bakåtläckage av blod in i kranskärlssystemet under förmakssystole.
Anatomiska variationer
Koronardominans
Begreppet koronardominans definieras utifrån vilket kranskärl som avger ramus interventricularis posterior (PDA) och därmed står för den huvudsakliga blodförsörjningen till det bakre interventrikulärseptumet och vänster kammares inferiora vägg.
- Högerdominans: Förekommer hos cirka 85 % av befolkningen och innebär att PDA utgår från höger kranskärl (RCA).
- Vänsterdominans: Förekommer hos cirka 8–10 % av individerna. PDA utgår i dessa fall från ramus circumflexus (LCx).
- Kodominans: Ett mönster som ses hos ungefär 5–7 % av populationen, där blodförsörjningen till PDA-territoriet delas och mottar bidrag från både RCA och LCx.
Anomala kranskärlsavgångar
Medfödda anomalier avseende kranskärlens avgång från aortaroten utgör viktiga, och i vissa fall livshotande, anatomiska avvikelser.
- ALCAPA (Anomalous Left Coronary Artery from the Pulmonary Artery): En sällsynt medfödd missbildning med en incidens på cirka 1 på 300 000 levande födda. Vid ALCAPA utgår den vänstra huvudstammen (LCA) felaktigt från lungartären (truncus pulmonalis) istället för från vänster sinus aortae. Detta leder till allvarliga störningar i hjärtats perfusionsdynamik postnatalt i takt med att trycket i lungcirkulationen sjunker.
- Enkelt kranskärl (Single coronary artery): En mycket ovanlig variant med en prevalens på 0,024–0,066 % vid angiografiska studier. Tillståndet innebär att ett enda kärl försörjer hela myokardiet. Kärlet förgrenar sig ofta för att imitera ett normalt dualt system, men anomalin kan medföra stora ischemiska risker beroende på kärlets exakta förlopp.
Variationer i kranskärlens förlopp
Kranskärlens epikardiella förlopp uppvisar ibland anatomiska avvikelser som kan ha klinisk relevans:
- Myokardbryggor (Myocardial bridging): Innebär att ett segment av en i övrigt epikardiell artär löper intramuralt (inuti myokardiet). Tillståndet drabbar oftast den mellersta tredjedelen av LAD. Prevalensen uppskattas till 2–7 % vid invasiv angiografi, men fynd i obduktionsserier på över 30 % indikerar en betydande underdiagnostik in vivo.
- Hög avgång (High takeoff): Definieras som att kranskärlsostierna är belägna mer än 5 mm ovanför den sinotubulära övergången i aorta. Det är ett sällsynt bifynd (incidens ca 0,2 %) som saknar fysiologisk påverkan men som kan försvåra hjärtkirurgiska eller interventionella (kateterbaserade) ingrepp.
Embryologisk och genetisk bakgrund
Den embryologiska grunden till dessa anatomiska variationer etableras under hjärtats tidiga morfogenes. Koronardominansen fastställs genom tillväxten hos proepikardiellt deriverade endotelceller och deras anslutning till aortaroten, vilket i sin tur avgör huruvida RCA eller LCx förlängs för att bilda PDA. Missbildningar som ALCAPA uppstår sannolikt som en följd av defekt septumbildning eller felaktig migration av kranskärlsanlagen från truncus pulmonalis under gestationsvecka 5 till 7.
Förekomsten av dessa anatomiska varianter påverkas även av kön och etnicitet, vilket belyser den underliggande genetiska styrningen. Studier har visat subtila könsskillnader; exempelvis är vänsterdominans något vanligare hos kvinnor (cirka 10–12 %) jämfört med män i vissa populationer, även om de övergripande dominansmönstren förblir relativt konstanta över könsgränserna.
Koronarperfusion (Koronart blodflöde)
Det fasiska flödesmönstret och diastolisk dominans
Det koronara blodflödet uppvisar ett unikt, fasiskt mönster som är strikt synkroniserat med hjärtcykeln. Detta skiljer kranskärlscirkulationen markant från den systemiska cirkulationen, framför allt på grund av de mekaniska begränsningar som uppstår när myokardiet kontraherar. I vänster kammare sker 70–80 % av det totala blodflödet under diastole. När myokardiet relaxerar sjunker spänningen (tensionen) i kammarväggen avsevärt. Denna tryckminskning lättar på kompressionen av de intramurala kärlen och möjliggör ett obehindrat inflöde och maximal perfusion från aortaroten.
Systolisk impedans
Under systole är det koronara blodflödet till vänster kammare kraftigt reducerat eller nästan helt avstannat. Detta fenomen, benämnt systolisk impedans, är mest uttalat i de subendokardiella lagren. Under kontraktionen överstiger det intramurala trycket i vänster kammare det diastoliska trycket i aorta, vilket komprimerar mikrocirkulationen och hindrar ett framåtriktat flöde. I svåra fall kan de kompressiva krafterna till och med leda till en övergående reversering av flödet (bakåtflöde).
Hemodynamiska skillnader i höger kammare
Höger kammare uppvisar en annorlunda hemodynamisk profil med en betydligt mindre uttalad diastolisk dominans, där endast cirka 50 % av flödet sker under diastole. Den fysiologiska förklaringen är att höger kammares tunnare myokardvägg genererar ett väsentligt lägre intramuralt tryck. Den svagare systoliska kompressionen av högerkammarens kärlbädd tillåter därmed en mer kontinuerlig perfusion genom hela hjärtcykeln.
Klinisk utvärdering av flödesmönster
Kranskärlens fasiska flödesmönster kan utvärderas med invasiva metoder som koronarangiografi eller intravaskulär tryck- och flödesmätning (exempelvis med Doppler-ledare). En frisk koronarartär uppvisar karakteristiska toppar i den diastoliska flödeshastigheten, vilket kliniskt ofta kvantifieras som en diastolisk-systolisk hastighetskvot. Hos ett friskt kärl överstiger denna kvot normalt 1,5.
Hjärtfrekvensens påverkan och koronar flödesreserv (CFR)
Vid takykardi (förhöjd hjärtfrekvens) förkortas hjärtcykelns diastoliska fas oproportionerligt mycket i förhållande till systole. Detta reducerar den totala tid som vänster kammare har tillgänglig för sitt huvudsakliga blodflöde, vilket riskerar att begränsa den myokardiella syrgasleveransen vid ansträngning.
För att möta myokardiets ökade metabola behov förlitar sig hjärtat på den koronara flödesreserven (Coronary Flow Reserve, CFR). CFR definieras som kvoten mellan maximalt (hyperemiskt) och basalt myokardiellt blodflöde. Hos friska individer uppgår CFR normalt till mellan 3 och 5, vilket speglar koronarkärlens förmåga att via vasodilatation kraftigt öka perfusionen och övervinna cykelns mekaniska begränsningar vid stress.
Reglering av koronarperfusion
Det koronara blodflödet är strikt reglerat för att exakt matcha myokardiets syrgasbehov, vilket fluktuerar kraftigt beroende på hjärtats aktuella arbetsbelastning. Regleringen utgörs av ett komplext samspel mellan intrinsiska (lokala) mekanismer, såsom autoreglering och metabol kontroll, och extrinsiska faktorer, som neural och hormonell modulering. Detta säkerställer adekvat perfusion och förhindrar ischemi trots varierande blodtryck och metabola krav.
Autoreglering och den myogena responsen
Autoreglering är en basal intrinsisk mekanism som upprätthåller ett relativt konstant koronarflöde oberoende av systemiska blodtrycksvariationer, förutsatt att perfusionstrycket (vanligen systemiskt medelartärtryck) ligger mellan cirka 60 och 180 mmHg. Denna stabilitet uppnås primärt genom den myogena responsen: när det transmurala trycket ökar, kontraherar den glatta muskulaturen i koronarkärlens arterioler för att öka resistensen, och när trycket sjunker sker en relaxation. Vid trycknivåer under 60 mmHg eller över 180 mmHg överskrids autoregleringskapaciteten, och blodflödet blir istället linjärt tryckberoende.
Metabol kontroll
Den metabola kontrollen är den enskilt mest dominanta regulatorn av det koronara blodflödet. Den kopplar perfusionen direkt till myokardiets syrgaskonsumtion genom att frisätta potenta vasodilaterande substanser vid vävnadshypoxi eller ökat hjärtarbete. De viktigaste mediatorerna inkluderar:
- Adenosin: En nedbrytningsprodukt av ATP som frisätts vid hög energiförbrukning. Adenosin binder till $A_2$-receptorer i kärlväggen och inducerar kraftig dilatation av arteriolerna.
- Kväveoxid (NO): Genereras av endotelialt kväveoxidsyntas (eNOS) och medierar relaxation av den underliggande glatta muskulaturen.
- Extracellulära kaliumjoner ($K^+$): Frisätts under metabol stress och inducerar hyperpolarisering av den vaskulära glatta muskulaturen (via s.k. inward rectifier-kanaler), vilket leder till kärlvidgning.
Endotelial reglering (Flödesmedierad vasodilatation)
Kranskärlens endotel finjusterar den vaskulära tonusen genom att reagera på hemodynamiska krafter. Ökad skjuvstress (shear stress) på kärlväggen, som uppstår när blodflödet ökar, stimulerar eNOS till ökad frisättning av NO. Detta fenomen kallas flödesmedierad vasodilatation (FMD) och verkar i synergi med metabola signaler för att underlätta och upprätthålla en hög perfusionsvolym vid ansträngning.
Neural och autonom kontroll
Det autonoma nervsystemet utövar en extrinsisk modulering av kranskärlen, där det sympatiska nervsystemet är mest framträdande:
- Sympatikus: Aktivering av $\alpha_1$-adrenerga receptorer på den vaskulära glatta muskulaturen framkallar initialt en vasokonstriktion. Under fysisk ansträngning ”överröstas” dock denna effekt snabbt av den kraftiga metabola vasodilatationen (ett fenomen som kallas funktionell sympatolys). Samtidigt bidrar sympatisk $\beta$-adrenerg stimulering till vasodilatation genom ökat intracellulärt cAMP och minskat kalcium.
- Parasympatikus: Innervering via Nervus vagus spelar en mindre dominant roll, men inducerar en mild vasodilatation som primärt medieras via endotelial NO-frisättning.
Flödes-metabolism-koppling och myokardiellt syrgasbehov ($MVO_2$)
Kopplingen mellan flöde och metabolism innebär att perfusionen dikteras av det myokardiella syrgasbehovet ($MVO_2$). De centrala determinanterna för $MVO_2$ kan förenklat beskrivas med formeln:
$MVO_2 \approx \text{Hjärtfrekvens} \times \text{Kontraktilitet} \times \text{Väggspänning}$
Betydelsen av väggspänningen (wall tension) härleds ur Laplaces lag, där väggspänningen är direkt proportionell mot det intraventrikulära trycket och kavitetsradien, och omvänt proportionell mot väggtjockleken. En fysiologisk ökning i någon av dessa parametrar (t.ex. ökad hjärtfrekvens eller inotropi vid ansträngning) höjer omedelbart $MVO_2$ och utlöser en kompensatorisk, metabolt driven vasodilatation.
Perfusion av specialiserade strukturer
Det koronara blodflödet till hjärtats anatomiska specialstrukturer uppvisar unika mönster som är av avgörande klinisk betydelse, särskilt vid ischemisk hjärtsjukdom.
Papillarmusklernas blodförsörjning och sårbarhet
Mitralisklaffens papillarmuskler har en specifik och anatomiskt asymmetrisk blodförsörjning, vilket direkt påverkar deras sårbarhet för ischemi:
- Den anterolaterala papillarmuskeln: Försörjs i regel av en dubbel (dual) blodcirkulation via grenar från både left anterior descending (LAD) och arteria circumflexa (LCx). Denna dubbla försörjning ger muskeln en relativ resistens mot ischemi och infarkt.
- Den posteromediala papillarmuskeln: Försörjs i de flesta fall av en enda artär, posterior descending artery (PDA). Vid ett högerdominant kranskärlssystem (vilket ses hos cirka 85 % av befolkningen) utgår PDA från höger kranskärl (RCA). Detta gör den posteromediala papillarmuskeln ytterst sårbar för ocklusion i ett enskilt kärl.
Ischemi eller infarkt i dessa strukturer kan leda till papillarmuskeldysfunktion eller i värsta fall papillarmuskelruptur. Detta medför förlorad förankring (tension) i chordae tendineae och resulterar i en livshotande akut mitralisinsufficiens.
Retledningssystemets perfusion
Hjärtats retledningssystem är helt beroende av specifika artärgrenar, och anatomiska normalvarianter påverkar risken för att utveckla arytmier vid kranskärlssjukdom:
- Sinusknutan (SA-noden): Sinusknuteartären försörjer SA-noden och angränsande förmaksmyokard. Hos cirka 55 % av individerna avgår den från RCA, och hos resterande 45 % från LCx. Förmaksarytmier kan därmed uppstå vid både höger- och vänstersidig kranskärlssjukdom.
- AV-knutan (AV-noden): AV-nodartären är kritisk för impulsöverledningen till kamrarna. Hos cirka 90 % av befolkningen utgår den från RCA som en terminal gren nära hjärtats crux. Detta gör AV-noden särskilt känslig för inferior (högersidig) ischemi.
Både sinus- och AV-nodartären är fysiologiska ändartärer med mycket begränsat kollateralflöde, vilket gör att ocklusiva händelser snabbt ger påtagliga effekter på hjärtats retledningsförmåga.
Transmurala perfusionsgradienter och subendokardiell ischemi
Det existerar en påtaglig perfusionsgradient över myokardväggen, vilket skapar en regional sårbarhet. Subendokardiet (det inre muskellagret, vilket även innefattar djupare papillarmuskel- och nodalvävnad) är utsatt för de högsta kompressionskrafterna och den största väggstressen under systole.
För att möta detta har det subendokardiella myokardiet en betydligt högre basal syrgasextraktion (cirka 80–85 %) jämfört med subepikardiet (cirka 70 %). Eftersom syrgasextraktionen redan i vila är maximal, kan subendokardiet inte öka syreupptaget nämnvärt vid ökade behov. Denna gradient gör subendokardiet extremt känsligt för hypoperfusion; sjunker det koronara perfusionstrycket är subendokardiet den första vävnaden som drabbas av ischemi.
Hjärtklaffarnas och chordae tendineas mikrocirkulation
Själva hjärtklaffarnas segel (flikar) är i huvudsak avaskulära. De får sin näring och syrgas primärt via diffusion från blodet som passerar genom hjärtkaviteterna. I klaffarnas baser och anulus fibrosus finns dock en begränsad kärlförsörjning från angränsande koronargrenar och vasa vasorum. Chordae tendineae får sin blodförsörjning från små mikrovaskulära utlöpare som härstammar från papillarmusklernas artärer. Denna glesa kärlförsörjning medför en mycket begränsad regenerationsförmåga vid skada.
Kliniska konsekvenser av nodal ischemi
Direkt hypoperfusion av retledningssystemets specialiserade myocyter leder till ischemi som kan störa den elektriska stabiliteten:
- Ocklusion av sinusknuteartären: Kan orsaka uttalad sinusknutedysfunktion, vilket ofta manifesteras som symtomgivande bradykardi eller olika former av förmakstakyarytmier.
- Ocklusion av AV-nodartären: Orsakar fördröjd eller blockerad överledning som resulterar i AV-block av grad I, II eller III. Detta är en vanlig och allvarlig komplikation i samband med en inferior myokardinfarkt.
Diagnostik och behandling (FFR, iFR, iwFR)
För att diagnostisera störningar i koronarcirkulationen används en kombination av icke-invasiva och invasiva tekniker. Målet är att identifiera anatomiska obstruktioner, utvärdera ischemi och bedöma funktionell nedsättning.
Anatomisk och invasiv avbildning
- Kranskärlsangiografi (KAG): Den invasiva guldstandarden för visualisering av kranskärlens anatomi. KAG ger högupplösta bilder av luminella förträngningar och möjliggör en omedelbar terapeutisk åtgärd (intervention) i samma seans.
- Datortomografi av kranskärlen (CCTA): Ett icke-invasivt alternativ som ger detaljerade tredimensionella rekonstruktioner av hjärtats kärl. Metoden har ett utmärkt negativt prediktivt värde (NPV) och är särskilt effektiv för att utesluta signifikant kranskärlssjukdom hos patienter med låg till intermediär risk.
Ischemidiagnostik
Metoder som nuklearmedicinsk myokardscintigrafi (SPECT/PET) används för att utvärdera inducerbar ischemi. Genom att jämföra det myokardiella blodflödet i vila med flödet under provokation (fysisk eller farmakologisk belastning) kan man riskstratifiera symtomatiska individer som saknar känd kranskärlssjukdom.
Funktionell och intravaskulär bedömning
Anatomisk bedömning måste ofta kompletteras med funktionell utvärdering för att avgöra en stenos hemodynamiska betydelse:
- Fraktionell flödesreserv (FFR): Mätning av tryckskillnaden över en stenos under invasiv angiografi. Ett FFR-värde < 0,80 indikerar en fysiologiskt signifikant ischemi och utgör en stark indikation för intervention.
- Intravaskulärt ultraljud (IVUS): En kateterburen ultraljudsundersökning som ger tvärsnittsbilder av själva kärlväggen. Möjliggör detaljerad vävnadskaraktärisering av placket (t.ex. om det är lipidrikt, fibröst eller förkalkat) och bedömning av kärlremodellering, vilket är ovärderligt vid komplex procedurplanering.
Behandlingsstrategier och revaskularisering
Syftet med behandlingen är att återställa blodflödet, lindra symtom och förhindra ogynnsamma kardiovaskulära händelser.
- Perkutan koronarintervention (PCI): Kateterburen ballongvidgning med insättning av en läkemedelsavgivande stent (DES). Det är den föredragna metoden vid enskärlssjukdom samt vid selekterad flerkärlssjukdom, och förbättrar effektivt prognos och symtom i både akuta (AKS) och stabila skeenden.
- Kranskärlsoperation (CABG – Coronary Artery Bypass Grafting): Öppen hjärtkirurgi där man använder arteriella eller venösa grafter för att leda blodet förbi stenoserna. CABG ger en överlägsen långtidsöverlevnad jämfört med PCI vid komplex flerkärlssjukdom, i synnerhet hos patienter med diabetes mellitus eller vid signifikanta stenoser i vänster huvudstam.
Farmakoterapi och sekundärprevention
Läkemedelsbehandling är av central betydelse efter diagnosticerad kranskärlssjukdom eller genomgången intervention:
- Trombocythämning: Dubbel trombocythämmande behandling (DAPT) bestående av acetylsalicylsyra (ASA, 75–162 mg/dag) och en P2Y12-hämmare (t.ex. klopidogrel 75 mg/dag) rekommenderas för att minska risken för trombotiska händelser under minst 12 månader efter en PCI. Därefter rekommenderas oftast livslång monoterapi med ASA som fortsatt skydd.
- Lipidsänkning: Statiner används med målet att stabilisera aterosklerotiska plack och kraftigt sänka LDL-kolesterolet (riktmärke < 70 mg/dL, motsvarande ca 1,8 mmol/L), vilket dramatiskt sänker risken för återkommande ischemi.
- Betablockerare: Sänker hjärtats syrgasbehov genom att dämpa puls och kontraktilitet. De är kritiska efter en akut hjärthändelse, men enligt riktlinjer från 2023 betonas deras rutinmässiga långtidsanvändning mindre hos patienter med stabil kronisk kranskärlssjukdom som helt saknar hjärtsvikt eller nedsatt vänsterkammarfunktion.
Innovationer och mikrovaskulär dysfunktion
Den medicinska utvecklingen adresserar kontinuerligt begränsningarna hos befintliga behandlingar:
- Bioresorberbara stentar (Bioresorbable scaffolds): Dessa stentar, i motsats till permanenta metallstentar, bryts ned och försvinner från kärlväggen under en period av 2–3 år. Detta låter kärlet återfå sin naturliga dynamiska funktion (vasomotion) och kan på sikt minska risken för sen stenttrombos. De allra senaste generationerna (2025) visar förbättrad säkerhet och effekt i utvalda lesioner.
- Koronar mikrovaskulär dysfunktion (CMD): Ett växande fält gällande patienter som upplever svår angina pectoris trots helt normala (öppna) epikardiella kranskärl. Genom att kvantifiera den myokardiella blodflödesreserven med t.ex. Positronemissionstomografi (PET), kan ischemi på grund av störd mikrocirkulation påvisas. Identifiering av CMD vägleder till riktade medicinska terapier, såsom mer potenta vasodilaterare.
Fysiologisk utvärdering av kranskärlsstenoser
När man vid en kranskärlsröntgen (angiografi) upptäcker en stenos (förträngning) som är visuellt ”intermediär” – det vill säga cirka 40–70 % förträngning av kärlets diameter – kan det vara mycket svårt att med blotta ögat avgöra om stenosen faktiskt hämmar blodflödet tillräckligt mycket för att orsaka ischemi. För att undvika onödiga stentinläggningar (PCI) eller att missa behandlingskrävande stenoser, använder man tryckmätning via en särskild ledare (guidewire) direkt i kranskärlet.
De två primära metoderna för detta är FFR och iFR (ofta även förkortat iwFR). Båda metoderna har högsta rekommendationsgrad i internationella och svenska riktlinjer för att vägleda beslut om revaskularisering.
1. FFR (Fractional Flow Reserve)
Vad är det?
FFR är den ursprungliga ”guldstandarden” för invasiv fysiologisk bedömning. Metoden mäter förhållandet mellan trycket distalt om (efter) stenosen och trycket i aortaroten (före stenosen) under maximalt blodflöde.
Hur fungerar det?
För att mäta FFR krävs att hjärtats mikrocirkulation är maximalt vidgad (maximal hyperemi) så att det perifera motståndet är så lågt som möjligt. Detta uppnås genom att man administrerar ett kärlvidgande läkemedel, oftast adenosin, antingen intravenöst eller direkt i kranskärlet (intrakoronart).
- Formel: FFR = $P_d / P_a$ (distalt tryck dividerat med aortatryck under hyperemi).
- Ett FFR-värde på 0,80 innebär att blodflödet förbi stenosen är reducerat till 80 % av vad det skulle ha varit utan stenosen.
Kliniskt gränsvärde (Cut-off):
- FFR $\le$ 0,80: Indikerar en fysiologiskt signifikant stenos som orsakar ischemi. Här rekommenderas revaskularisering (oftast PCI med stent).
- FFR > 0,80: Indikerar att stenosen sannolikt inte är ischemi-drivande, och patienten behandlas bäst med enbart medicinering.
2. iFR / iwFR (Instantaneous Wave-free Ratio)
Vad är det?
iFR (ibland skrivet iwFR) är en nyare mätmetod som mäter exakt samma tryckskillnader som FFR, men utan att man behöver ge något kärlvidgande läkemedel.
Hur fungerar det?
iFR utnyttjar en fysiologisk princip. Under en specifik och kort del av hjärtats vilofas (den diastoliska ”wave-free”-perioden) är det mikrovaskulära motståndet i hjärtat naturligt minimerat och extremt stabilt. Genom att enbart mäta och beräkna tryckkvoten under just denna bråkdel av en sekund, får man fram ett värde som korrelerar mycket väl med FFR, fast under vilande förhållanden.
- Ingen farmakologisk stress krävs: Eftersom man mäter i denna specifika fas behövs inget adenosin.
Kliniskt gränsvärde (Cut-off):
- iFR / iwFR $\le$ 0,89: Indikerar en fysiologiskt signifikant stenos som bör åtgärdas.
- iFR / iwFR > 0,89: Indikerar att stenosens påverkan är mild och intervention inte behövs.
Klinisk användning och val av metod
Varför använda dessa tekniker?
Innan dessa metoder fanns led den interventionala kardiologin av den så kallade ”okulo-stenotiska reflexen” – ser man en stenos vill man stenta den. FFR och iFR har bevisat att många till synes allvarliga stenoser faktiskt inte påverkar flödet, och att sätta in en stent i ett sådant kärl utsätter patienten för onödiga risker (stenttrombos, blödningar via blodförtunnande mediciner) utan att ge någon symtom- eller överlevnadsvinst. Å andra sidan kan diffusa stenoser som ser oskyldiga ut på röntgen visa sig vara mycket ischemi-drivande när de mäts.
FFR vs. iFR – vad väljer man?
Stora kliniska landmärkesstudier (bland annat den stora svenskledda studien iFR-SWEDEHEART och studien DEFINE-FLAIR) har visat att iFR är precis lika säkert och effektivt för att styra behandlingen som FFR när det gäller långtidsöverlevnad och risk för nya hjärtinfarkter.
Idag har iFR/iwFR (samt andra liknande vilande tryckindex som t.ex. RFR eller dPR) i stor utsträckning tagit över som förstahandsval på många lab. Anledningarna är flera:
- Patientkomfort: Adenosin (som används vid FFR) ger ofta övergående men mycket obehagliga biverkningar som tryck över bröstet (nära på ”infarktkänsla”), andnöd och blodtrycksfall. iFR slipper detta helt.
- Tidseffektivitet: Att slippa bereda och administrera läkemedel sparar tid under proceduren.
- Specifika patientgrupper: Hos patienter med uttalad astma är adenosin kontraindicerat på grund av risken för bronkospasm, varför iFR är ett utmärkt alternativ.
FFR används dock fortfarande flitigt, särskilt i gränsfall eller om vilotillståndet av någon anledning misstänks ge en felaktig bild. Ofta används en hybridstrategi där iFR genomförs först; hamnar värdet väldigt nära gränsen (t.ex. 0,90) kan operatören välja att komplettera med adenosin och ett FFR-värde för att vara helt säker.
Referenser
- https://www.osmosis.org/learn/Coronary_circulation
- https://www.vhlab.umn.edu/atlas/physiology-tutorial/coronary-circulation.shtml
- https://www.hopkinsmedicine.org/health/conditions-and-diseases/anatomy-and-function-of-the-coronary-arteries
- https://www.ncbi.nlm.nih.gov/books/NBK549786/
- https://www.ncbi.nlm.nih.gov/books/NBK534790/
- https://www.ncbi.nlm.nih.gov/books/NBK537357/
- https://www.ahajournals.org/doi/10.1161/atvbaha.112.300717
- https://pmc.ncbi.nlm.nih.gov/articles/PMC7029210/
- https://www.ncbi.nlm.nih.gov/books/NBK482375/
- https://pmc.ncbi.nlm.nih.gov/articles/PMC6205847/
- https://www.ahajournals.org/doi/10.1161/JAHA.123.032851
- https://pmc.ncbi.nlm.nih.gov/articles/PMC11586415/
- https://www.ahajournals.org/doi/10.1161/JAHA.124.039013
- https://www.ncbi.nlm.nih.gov/books/NBK557566/
- https://www.vhlab.umn.edu/atlas/cardiac-veins/coronary-sinus/index.shtml
- https://www.vhlab.umn.edu/atlas/cardiac-veins/coronary-sinus-ostium/index.shtml
- https://www.vhlab.umn.edu/atlas/cardiac-veins/index.shtml
- https://www.ncbi.nlm.nih.gov/books/NBK541040/
- https://anatomy.elpaso.ttuhsc.edu/anatomytables/veins_thorax.html
- https://pmc.ncbi.nlm.nih.gov/articles/PMC4486412/
- https://pubmed.ncbi.nlm.nih.gov/19587062/
- https://academic.oup.com/ehjcr/article/2/2/yty070/5042355
- https://pmc.ncbi.nlm.nih.gov/articles/PMC12060931/
- https://medcraveonline.com/JCCR/morphology-of-coronary-arteries-in-relation-to-ischemic-heart-disease.html
- https://www.ahajournals.org/doi/10.1161/01.cir.0000065118.99409.5f
- https://pubmed.ncbi.nlm.nih.gov/21322035/
- https://onlinelibrary.wiley.com/doi/10.1002/ca.21088
- https://pmc.ncbi.nlm.nih.gov/articles/PMC2132202/
- https://www.nature.com/articles/s41598-020-71174-9
- https://anatomypubs.onlinelibrary.wiley.com/doi/10.1002/ar.24951
- https://academic.oup.com/eurheartj/article/34/34/2674/617228
- https://pubmed.ncbi.nlm.nih.gov/10933379/
- https://www.ahajournals.org/doi/10.1161/circ.142.suppl_3.15360
- https://www.jacc.org/doi/10.1016/j.jcmg.2021.07.009
- https://pmc.ncbi.nlm.nih.gov/articles/PMC6701300/
- https://pmc.ncbi.nlm.nih.gov/articles/PMC9653150/
- https://pmc.ncbi.nlm.nih.gov/articles/PMC4919754/
- https://academic.oup.com/cardiovascres/article/109/2/204/2196618
- https://www.ahajournals.org/doi/10.1161/circulationaha.121.055347
- https://pmc.ncbi.nlm.nih.gov/articles/PMC10811496/
- https://pmc.ncbi.nlm.nih.gov/articles/PMC5966026/
- https://derangedphysiology.com/main/cicm-primary-exam/cardiovascular-system/Chapter-476/coronary-blood-flow
- https://pmc.ncbi.nlm.nih.gov/articles/PMC9724998/
- https://eurointervention.pcronline.com/article/phasic-flow-patterns-of-right-versus-left-coronary-arteries-in-patients-undergoing-clinical-physiological-assessment
- https://pmc.ncbi.nlm.nih.gov/articles/PMC2438254/
- https://pubmed.ncbi.nlm.nih.gov/1381797/
- https://onlinelibrary.wiley.com/doi/10.1002/cphy.c160016
- https://pmc.ncbi.nlm.nih.gov/articles/PMC5974144/
- https://pmc.ncbi.nlm.nih.gov/articles/PMC7165467/
- https://pmc.ncbi.nlm.nih.gov/articles/PMC11607609/
- https://pubmed.ncbi.nlm.nih.gov/9588871/
- https://www.ahajournals.org/doi/10.1161/01.cir.103.13.1752
- https://www.ncbi.nlm.nih.gov/books/NBK499897/
- https://cvphysiology.com/cad/cad004
- https://pmc.ncbi.nlm.nih.gov/articles/PMC11096616/
- https://www.openanesthesia.org/keywords/coronary-artery-anatomy-and-coronary-perfusion-pressure/
- https://pmc.ncbi.nlm.nih.gov/articles/PMC8086776/
- https://radiopaedia.org/articles/sinoatrial-nodal-artery?lang=us
- https://www.cureus.com/articles/138981-anatomical-study-of-the-atrioventricular-nodal-branch-of-the-heart
- https://www.ncbi.nlm.nih.gov/books/NBK541008/
- https://s.mriquestions.com/uploads/3/4/5/7/34572113/cardiac_physiology_review_article_2015.pdf
- https://pmc.ncbi.nlm.nih.gov/articles/PMC3064294/
- https://www.ncbi.nlm.nih.gov/books/NBK557656/
- https://www.ahajournals.org/doi/10.1161/circulationaha.116.018011
- https://ecgwaves.com/topic/conduction-defects-myocardial-ischemia-infarction/
- https://www.ncbi.nlm.nih.gov/books/NBK554410/
- https://www.ahajournals.org/doi/10.1161/circresaha.114.302721
- https://www.ncbi.nlm.nih.gov/books/NBK507799/
- https://www.merckmanuals.com/professional/cardiovascular-disorders/arteriosclerosis/atherosclerosis
- https://www.nature.com/articles/s41572-019-0106-z
- https://academic.oup.com/eurheartj/article/32/10/1251/563574
- https://www.cdc.gov/heart-disease/risk-factors/index.html
- https://www.heart.org/en/health-topics/consumer-healthcare/what-is-cardiovascular-disease/coronary-artery-disease
- https://bmcpublichealth.biomedcentral.com/articles/10.1186/s12889-019-7948-x
- https://www.ncbi.nlm.nih.gov/books/NBK459157/
- https://www.heart.org/en/health-topics/heart-attack/about-heart-attacks/acute-coronary-syndrome
- https://www.merckmanuals.com/professional/cardiovascular-disorders/coronary-artery-disease/overview-of-acute-coronary-syndromes-acs
- https://www.ahajournals.org/doi/10.1161/01.cir.92.3.657
- https://pubmed.ncbi.nlm.nih.gov/10729375/
- https://www.jacc.org/doi/10.1016/j.jacc.2023.03.391
- https://bmccardiovascdisord.biomedcentral.com/articles/10.1186/s12872-025-05022-x
- https://pubmed.ncbi.nlm.nih.gov/30587416/
- https://pubmed.ncbi.nlm.nih.gov/15599567/
- https://pubmed.ncbi.nlm.nih.gov/26811390/
- https://pubmed.ncbi.nlm.nih.gov/38003878/
- https://pubmed.ncbi.nlm.nih.gov/38051412/
- https://pubmed.ncbi.nlm.nih.gov/16080979/
- https://pubmed.ncbi.nlm.nih.gov/37692750/
- https://pubmed.ncbi.nlm.nih.gov/23518380/
- https://www.ncbi.nlm.nih.gov/books/NBK470279/
- https://www.ahajournals.org/doi/10.1161/01.cir.0000080946.42225.4d
- https://www.ahajournals.org/doi/10.1161/circulationaha.115.018747
- https://www.ahajournals.org/doi/10.1161/01.cir.102.6.617
- https://www.ahajournals.org/doi/10.1161/CIR.0000000000001038
- https://www.ahajournals.org/doi/10.1161/cir.0b013e318235eb4d
- https://www.ahajournals.org/doi/10.1161/CIR.0000000000001168
- https://pmc.ncbi.nlm.nih.gov/articles/PMC9352968/
- https://journals.lww.com/annals-of-medicine-and-surgery/fulltext/2025/07000/bioresorbable_scaffolds_advances%2C_challenges%2C_and.28.aspx
- https://pmc.ncbi.nlm.nih.gov/articles/PMC6214157/

