Handläggning av förmaksflimmer och antikoagulationsbehandling
Introduktion och patofysiologiska mekanismer
Förmaksflimmer (FF) är fortfarande den vanligast förekommande ihållande hjärtarytmin inom klinisk kardiologi och utgör en betydande global hälsobörda. Det är i grunden en progressiv sjukdom som karakteriseras av desorganiserad, snabb och oregelbunden elektrisk aktivering i förmaken. Den nuvarande förståelsen av patofysiologin vid FF betonar ett komplext, dubbelriktat samspel mellan ektopiska elektriska triggers – som oftast har sitt ursprung i myokardstråk som sträcker sig in i lungvenerna – och ett sårbart arytmogent substrat [1]. Detta substrat drivs av både strukturell remodellering, inklusive förmaksdilatation och interstitiell fibros, och elektrisk remodellering, såsom förkortning av förmakets effektiva refraktärperiod. Denna självunderhållande cykel sammanfattas klassiskt av det elektrofysiologiska axiomet ”flimmer föder flimmer”.
Utöver de hemodynamiska konsekvenserna av förlorad atrioventrikulär synkroni är den allvarligaste komplikationen vid FF kardioembolisk stroke. Den trombogena potentialen vid FF förklaras elegant av Virchows triad. Förmakens mekaniska svikt, i synnerhet i det kraftigt trabekulerade vänstra förmaksörat (LAA), leder till uttalad blodstas. Samtidigt inducerar kronisk förmakssträckning och systemisk inflammation endoteldysfunktion, medan själva arytmin främjar ett systemiskt hyperkoagulabelt tillstånd [2]. Tromber som bildas i LAA är mycket benägna att embolisera systemiskt, vilket gör FF till en ledande orsak till allvarlig, invalidiserande ischemisk stroke. Följaktligen ligger hörnstenen i handläggningen av FF i den noggranna stratifieringen av tromboembolisk risk och den välavvägda användningen av antikoagulationsbehandling.
Diagnostik, riskstratifiering och paradigmskiftet gällande riskpoäng
Diagnostiska kriterier och sjukdomskontinuumet
Den kliniska diagnosen av FF kräver elektrokardiografisk dokumentation. Aktuella riktlinjer kräver ett standard 12-avlednings-EKG eller en enavlednings-EKG-registrering på minst 30 sekunder som påvisar oregelbundet oregelbundna RR-intervall i avsaknad av tydliga, repeterande P-vågor [1]. Med insikten om att FF inte bara är en isolerad elektrisk händelse utan en systemisk sjukdomsprocess, introducerade 2023 års ACC/AHA-riktlinjer en ny kontinuumklassificering: Stadium 1 (Risk för FF på grund av modifierbara riskfaktorer), Stadium 2 (Pre-FF, karakteriserat av strukturella eller elektriska fynd utan kliniskt FF), Stadium 3 (Kliniskt FF, underindelat i paroxysmalt, persisterande, långvarigt persisterande och framgångsrik ablation), och Stadium 4 (Permanent FF, där ytterligare försök till rytmkontroll har övergetts) [1].
Dilemmat med subkliniskt FF och AHRE
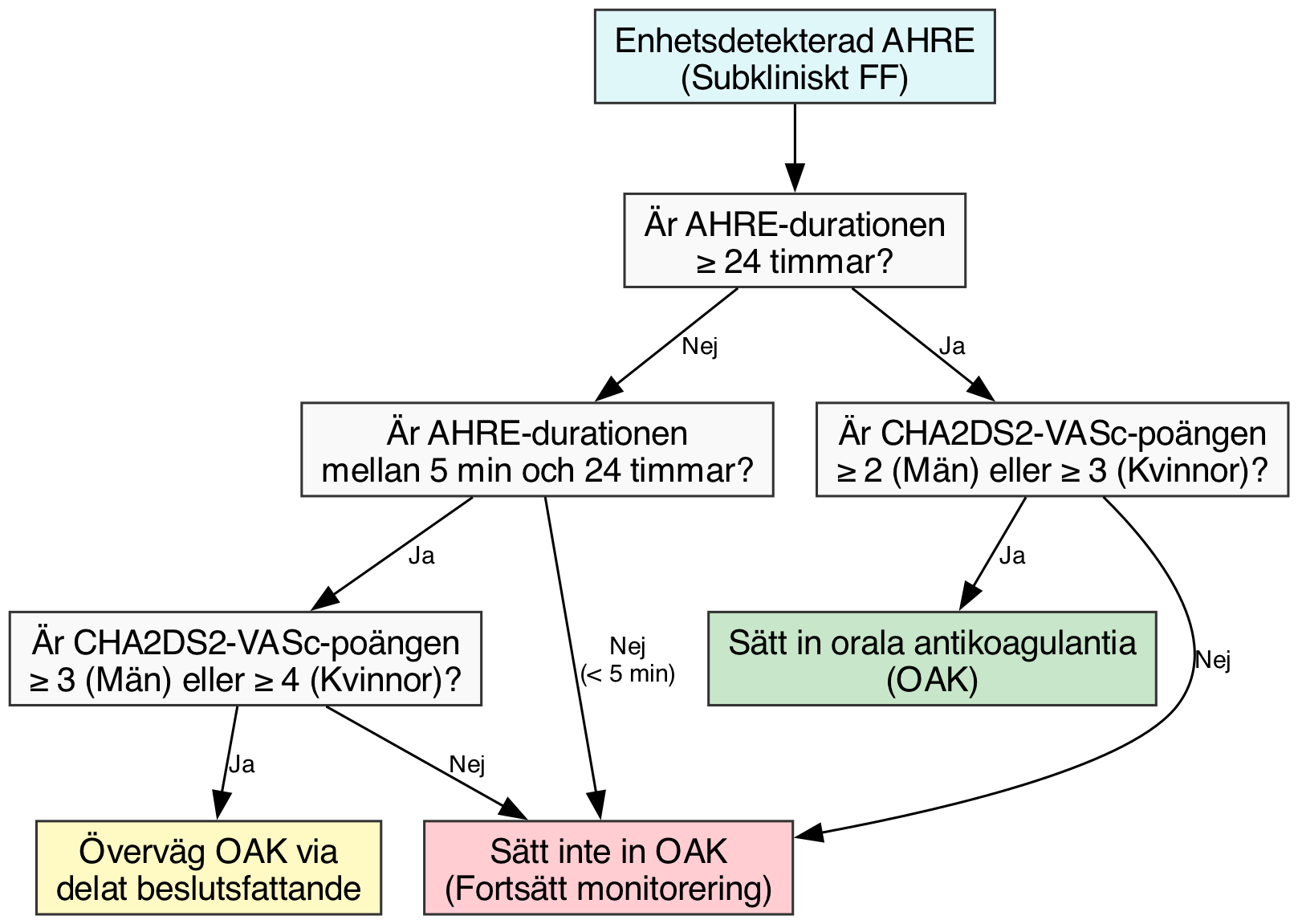
Den ökande användningen av implanterbara elektroniska hjärtutrustningar (CIED) och kroppsburna enheter (wearables) för konsumenter har introducerat det kliniska dilemmat med förmaksepisoder med hög frekvens (AHRE) eller subkliniskt FF. Handläggningen av dessa episoder är avhängig av deras duration och patientens underliggande tromboemboliska risk. Om en AHRE varar i 24 timmar eller längre hos en patient med minst 2 poäng enligt CHA₂DS₂-VASc rekommenderas starkt insättning av orala antikoagulantia (OAK). För episoder som varar mellan 5 minuter och 24 timmar hos patienter med en högriskprofil (CHA₂DS₂-VASc ≥ 3) kan OAK övervägas efter noggrant delat beslutsfattande (shared decision-making). Episoder som varar kortare tid än 5 minuter motiverar för närvarande inte systemisk antikoagulation [1].
Tromboembolisk risk och blödningsrisk
CHA₂DS₂-VASc-poängsystemet är fortsatt den allmänt accepterade guldstandarden för att predicera strokerisk vid FF. OAK rekommenderas starkt vid poäng ≥ 2 för män och ≥ 3 för kvinnor [1]. Strategin för stratifiering av blödningsrisk har dock genomgått ett radikalt paradigmskifte. Historiskt sett förlitade man sig i stor utsträckning på HAS-BLED-poäng för att kvantifiera blödningsrisken. Sentida riktlinjer, i synnerhet 2024 års riktlinjer från European Society of Cardiology (ESC), har frångått den isolerade användningen av strukturerade blödningspoäng. ESC har uttryckligen utelämnat HAS-BLED-poäng och betonar att en hög blödningsriskpoäng aldrig får användas som en ursäkt för att undanhålla livräddande OAK [2]. Istället har fokus flyttats mot en dynamisk, individualiserad bedömning av modifierbara blödningsriskfaktorer, såsom okontrollerad hypertoni, samtidig användning av icke-steroida antiinflammatoriska läkemedel (NSAID) eller trombocytaggregationshämmare, samt överdriven alkoholkonsumtion.
Grundläggande handläggning och DOAK-revolutionen
AF-CARE-ramverket
För att effektivisera den mångfacetterade handläggningen av FF introducerade 2024 års ESC-riktlinjer behandlingsalgoritmen ”AF-CARE” [2]. Detta holistiska ramverk prioriterar:
- Comorbidity and risk factor management (Hantering av komorbiditet och riskfaktorer): Betonar aggressiv viktnedgång (≥ 10 %), strikt blodtryckskontroll och integrering av SGLT2-hämmare vid samtidig hjärtsvikt.
- Avoid stroke and thromboembolism (Undvik stroke och tromboembolism): Optimering av OAK-behandling baserat på dynamiska riskbedömningar.
- Reduce symptoms (Minska symtom): Användning av strategier för frekvens- och rytmkontroll. Tidig rytmkontroll (via antiarytmika eller kateterablation) förordas i allt högre grad för att bromsa sjukdomsprogressionen, särskilt hos patienter med hjärtsvikt med nedsatt ejektionsfraktion (HFrEF) [1].
- Evaluation and dynamic reassessment (Utvärdering och dynamisk omprövning): Insikt om att FF och dess associerade risker utvecklas över tid.
Banbrytande evidens: DOAK jämfört med warfarin
Landskapet för strokeprevention vid icke-valvulärt FF förändrades oåterkalleligt i och med introduktionen av direkta orala antikoagulantia (DOAK), vilka inkluderar den direkta trombinhämmaren dabigatran och faktor Xa-hämmarna apixaban, rivaroxaban och edoxaban. De fyra avgörande randomiserade kontrollerade studierna – RE-LY (dabigatran) [4], ROCKET AF (rivaroxaban) [5], ARISTOTLE (apixaban) [6] och ENGAGE AF-TIMI 48 (edoxaban) [7] – fastställde kollektivt att DOAK är non-inferior, och i vissa fall överlägsna, vitamin K-antagonister (VKA) som warfarin för prevention av stroke och systemisk embolism.
Avgörande var att DOAK uppvisade en betydande säkerhetsfördel och konsekvent minskade risken för förödande intrakraniell blödning med cirka 50 % jämfört med warfarin. Denna säkerhetsprofil, i kombination med bekvämligheten av fast dosering utan behov av rutinmässig koagulationsmonitorering, har befäst DOAK som de allmänt föredragna förstahandsvalen vid icke-valvulärt FF. Den nyligen genomförda nätverksmetaanalysen COMBINE AF på individuell patientnivå, som poolade data från 71 683 patienter i dessa banbrytande studier, bekräftade definitivt den överlägsna säkerhets- och effektprofilen för DOAK över olika ålders- och könsdemografier, vilket förstärker deras grundläggande roll inom modern kardiologi [3].
Särskilda patientgrupper och kliniska kontroverser
Kronisk njursjukdom och terminal njursvikt
Handläggningen av FF hos patienter med avancerad kronisk njursjukdom (CKD) och terminal njursvikt (ESKD) i hemodialys är fortfarande ett område med uttalad klinisk osäkerhet (clinical equipoise). Patienter med ESKD lider av en paradoxal ökning av både tromboemboliska och blödningsrelaterade risker. De banbrytande DOAK-studierna exkluderade i stor utsträckning patienter med kreatininclearance under 25–30 ml/min. Nyligen genomförda studier som försökt klargöra detta område, inklusive RENAL-AF (apixaban) [9], AXADIA-AFNET 8 (apixaban) [10] och VALKYRIE (rivaroxaban) [11], visade att DOAK har en säkerhets- och effektprofil som är jämförbar med VKA hos hemodialyspatienter. Dessa studier var dock statistiskt underdimensionerade för att kunna bevisa definitiv överlägsenhet. Följaktligen, medan amerikanska FDA tillåter användning av apixaban vid ESKD baserat på farmakokinetiska data, bibehåller europeiska riktlinjer en mycket försiktig hållning. Kardiologkåren inväntar med spänning resultaten från stora pågående studier, såsom SAFE-D och DANWARD, vilka utvärderar DOAK jämfört med en strategi utan antikoagulation i denna sårbara kohort.
Valvulärt förmaksflimmer: INVICTUS-studien
Termen ”valvulärt FF” definieras strikt i aktuella riktlinjer som FF som uppträder i närvaro av en mekanisk hjärtklaffprotes eller måttlig till uttalad reumatisk mitralisstenos [1]. I dessa specifika scenarier är DOAK absolut kontraindicerade. Den patofysiologiska grunden belystes tydligt av INVICTUS-studien, som jämförde rivaroxaban med VKA-behandling hos patienter med reumatisk hjärtsjukdomsassocierat FF [8]. Studien avbröts i förtid efter att definitivt ha visat att VKA-behandling var vida överlägsen rivaroxaban, vilket resulterade i signifikant lägre frekvens av ischemisk stroke och mortalitet. Detta beror sannolikt på den unika patofysiologiska miljön vid reumatisk mitralisstenos, vilken orsakar uttalad mekanisk svikt i vänster förmak och massiv blodstas, vilket nödvändiggör den bredare, multifaktoriella koagulationshämningen som VKA ger snarare än den målsökning mot en enskild faktor som DOAK erbjuder.
Tidpunkt för DOAK efter stroke: Avveckling av ”1-3-6-12”-regeln
Historiskt sett fördröjde kardiologer och neurologer insättningen av OAK i 1 till 2 veckor efter en akut ischemisk stroke på grund av uttalad rädsla för hemorragisk transformation, och förlitade sig ofta på den godtyckliga ”1-3-6-12”-dagarsregeln baserat på strokens svårighetsgrad. Detta paradigm har helt skrivits om av data från nyligen genomförda studier. ELAN-studien visade att tidig DOAK-insättning (≤ 48 timmar vid lindrig/måttlig stroke, och dag 6–7 vid svår stroke) inte bara är säker utan även minskar incidensen av recidiverande ischemisk stroke utan att öka frekvensen av symtomatisk intrakraniell blödning jämfört med senare insättning [13]. Dessa fynd bekräftades nyligen av CATALYST-metaanalysen, vilket befäster tidig DOAK-insättning som den nya standardbehandlingen [14].

Ocklusion av vänster förmaksöra (LAA)
För patienter som inte tolererar långvarig OAK-behandling erbjuder mekanisk exklusion av LAA ett gångbart alternativ. Kirurgiskt gav LAAOS III-studien banbrytande evidens för att samtidig kirurgisk LAA-ocklusion under hjärtkirurgi som utförs på annan indikation, i kombination med pågående OAK, minskar risken för stroke med imponerande 33 % jämfört med enbart OAK [12]. Perkutan LAA-ocklusion (med enheter som Watchman FLX eller Amplatzer Amulet) är för närvarande reserverad för patienter med icke-valvulärt FF som har en absolut kontraindikation mot långvarig OAK eller en oacceptabelt hög, icke-modifierbar blödningsrisk [1].
Periprocedural handläggning och handläggning vid blödning
Den periprocedurala handläggningen av DOAK har förenklats avsevärt genom PAUSE-studien, som etablerade ett säkert, standardiserat protokoll för uppehåll utan behov av riskfylld heparin-bridging (överbryggande behandling) eller rutinmässig koagulationsprovtagning [15]. Enligt PAUSE-protokollet pausas DOAK 1 dag före ingrepp med låg blödningsrisk och 2 dagar före ingrepp med hög blödningsrisk (med förlängt uppehåll för dabigatran vid CKD). Denna strategi resulterade i en 30-dagarsfrekvens av allvarlig blödning på mindre än 2 % och strokefrekvens på mindre än 1 %.

I händelse av livshotande blödning under pågående DOAK-behandling finns nu specifika reverseringsmedel tillgängliga och rekommenderade: idarucizumab för reversering av dabigatran, och andexanet alfa för reversering av faktor Xa-hämmare (apixaban och rivaroxaban). Om dessa specifika medel inte är tillgängliga fungerar fyrfaktorkoncentrat (PCC) som standardbehandling för att återställa hemostasen [2].
Framtida riktningar och slutsatser
Landskapet för antikoagulation vid FF fortsätter att utvecklas snabbt. Även om DOAK representerar ett monumentalt framsteg jämfört med VKA, medför de fortfarande en icke försumbar risk för kliniskt relevant blödning. Nästa gränsland inom strokeprevention ligger i utvecklingen av faktor XIa-hämmare (t.ex. asundexian, milvexian). Genom att rikta in sig på den inre koagulationsvägen frikopplar dessa medel teoretiskt hemostas från trombos, vilket lovar att förhindra patologisk trombosbildning utan att försämra kroppens fysiologiska svar på kärlskada. Även om tidiga fas-studier har visat lovande resultat, inväntar kardiologkåren resultaten från massiva fas III-utfallsstudier (såsom OCEANIC- och LILAC-programmen) för att avgöra om faktor XIa-hämmare kommer att ersätta DOAK som den nya höjdpunkten inom antikoagulationsbehandling.
Sammanfattningsvis kräver handläggningen av förmaksflimmer en nyanserad, patientcentrerad strategi. Integreringen av AF-CARE-ramverket, den välavvägda användningen av DOAK, frångåendet av restriktiva blödningspoäng och det snabba anammandet av protokoll för tidig antikoagulation efter stroke representerar zenit av modern evidensbaserad kardiologi. I väntan på ytterligare data gällande ESKD-populationer och nya farmakologiska substanser förblir den noggranna tillämpningen av aktuella riktlinjer vårt mest potenta vapen mot FF-relaterad morbiditet och mortalitet.
- Joglar JA, Chung MK, Armbruster AL, et al. 2023 ACC/AHA/ACCP/HRS Guideline for the Diagnosis and Management of Atrial Fibrillation. J Am Coll Cardiol. 2024;83(1):109-279. DOI: 10.1016/j.jacc.2023.08.017
- Van Gelder IC, Rienstra M, Bunting KV, et al. 2024 ESC Guidelines for the management of atrial fibrillation. Eur Heart J. 2024;45(36):3314-3414. DOI: 10.1093/eurheartj/ehae176
- Carnicelli AP, Hong H, Connolly SJ, et al. Direct Oral Anticoagulants Versus Warfarin in Patients With Atrial Fibrillation: Patient-Level Network Meta-Analyses of Randomized Clinical Trials With Interaction Testing by Age and Sex. Circulation. 2022;145(4):242-255. DOI: 10.1161/CIRCULATIONAHA.121.056355
- Connolly SJ, Ezekowitz MD, Yusuf S, et al. Dabigatran versus Warfarin in Patients with Atrial Fibrillation (RE-LY). N Engl J Med. 2009;361(12):1139-1151. DOI: 10.1056/NEJMoa0905561
- Patel MR, Mahaffey KW, Garg J, et al. Rivaroxaban versus Warfarin in Nonvalvular Atrial Fibrillation (ROCKET AF). N Engl J Med. 2011;365(10):883-891. DOI: 10.1056/NEJMoa1009638
- Granger CB, Alexander JH, McMurray JJ, et al. Apixaban versus Warfarin in Patients with Atrial Fibrillation (ARISTOTLE). N Engl J Med. 2011;365(11):981-992. DOI: 10.1056/NEJMoa1107039
- Giugliano RP, Ruff CT, Braunwald E, et al. Edoxaban versus Warfarin in Patients with Atrial Fibrillation (ENGAGE AF-TIMI 48). N Engl J Med. 2013;369(22):2093-2104. DOI: 10.1056/NEJMoa1310907
- Connolly SJ, Karthikeyan G, Ntsekhe M, et al. Rivaroxaban in Rheumatic Heart Disease-Associated Atrial Fibrillation (INVICTUS). N Engl J Med. 2022;387(11):978-988. DOI: 10.1056/NEJMoa2209051
- Pokorney SD, Chertow GM, Al-Khalidi HR, et al. Apixaban for Patients With Atrial Fibrillation on Hemodialysis: A Multicenter Randomized Controlled Trial (RENAL-AF). Circulation. 2022;146(23):1735-1745. DOI: 10.1161/CIRCULATIONAHA.121.054990
- Reinecke H, Engelbertz C, Bauersachs R, et al. A Randomized Controlled Trial Comparing Apixaban With the Vitamin K Antagonist Phenprocoumon in Patients on Chronic Hemodialysis (AXADIA-AFNET 8). Circulation. 2023;147(4):296-309. DOI: 10.1161/CIRCULATIONAHA.122.062779
- De Vriese AS, Caluwé R, Pyfferoen L, et al. Safety and Efficacy of Vitamin K Antagonists versus Rivaroxaban in Hemodialysis Patients with Atrial Fibrillation: A Multicenter Randomized Controlled Trial (VALKYRIE). J Am Soc Nephrol. 2020;31(1):148-158. DOI: 10.1681/ASN.2019060579
- Whitlock RP, Belley-Cote EP, Paparella D, et al. Left Atrial Appendage Occlusion during Cardiac Surgery to Prevent Stroke (LAAOS III). N Engl J Med. 2021;384(22):2081-2091. DOI: 10.1056/NEJMoa2101897
- Fischer U, Koga M, Strbian D, et al. Early versus Later Anticoagulation for Stroke with Atrial Fibrillation (ELAN). N Engl J Med. 2023;388(26):2411-2421. DOI: 10.1056/NEJMoa2303048
- Tsivgoulis G, Katsanos AH, Sandset EC, et al. Early anticoagulation after stroke decreases recurrence without increasing bleeding in patients with atrial fibrillation (CATALYST). Lancet. 2025. (Presented at WSC 2024).
- Douketis JD, Spyropoulos CQ, Duncan J, et al. Perioperative Management of Patients With Atrial Fibrillation Receiving a Direct Oral Anticoagulant (PAUSE). JAMA Intern Med. 2019;179(11):1469-1478. DOI: 10.1001/jamainternmed.2019.2431

