Medfödda hjärtfel & GUCH (Grown Up Congenital Heart disease)
Kongenitala hjärtfel & GUCH
I Sverige föds årligen cirka 800-1000 barn med medfödda hjärtfel. Under årens gång har överlevnaden vid medfödda hjärtfel ökat dramatiskt, vilket resulterat i att prevalensen av medfödda hjärtfel i befolkningen har ökat. Ungefär 95% av alla som föds med ett medfött hjärtfel når vuxen ålder. I relativa termer har överlevnaden ökat mest bland de med de svåraste hjärtfelen. Uppskattningsvis finns drygt 40.000 GUCH-patienter i Sverige, vilket gör GUCH ungefär lika vanligt som typ 1 diabetes. GUCH står för Grown Up Congenital Heart disease och utgör den inriktning inom kardiologin som omhändertar vuxna med medfödda hjärtfel.
Idag upptäcks majoriteten av alla större hjärtfel tidigt under spädbarnsåren eller barndomen. Ju större defekt, desto tidigare sker upptäckten. Defekter som leder till reducerad syrgassaturation upptäcks effektivt med hjälp av screening med pulsoximetri (POX) under de första levnadsdagarna. Mindre defekter kan gå obemärkta förbi under många år. Emellertid kan större defekter upptäckas först i vuxen ålder.
Barn med medfödda hjärtfel omhändertas av neonatologer, barnkardiologer och vid behov barnhjärtkirurger. I vuxen ålder fortsätter omhändertagandet med fördel på en GUCH-klinik. I Sverige finns sju större GUCH-centra (Lund, Göteborg, Stockholm, Uppsala, Linköping, Umeå, Örebro).
Prevalens av medfödda hjärtfel
Enligt European Society for Cardiology kan man räkna med att 2800 vuxna per 1 miljon invånare har ett medfött hjärtfel och hälften av dessa har ett måttligt eller komplicerat hjärtfel (resterande tredjedel har ett lindrigt hjärtfel (Baumgartner et al). I Sverige föds uppskattningsvis 800-1000 barn årligen med ett medfött hjärtfel.
Ekokardiografi
Ekokardiografi är förstahandsval för diagnostik och uppföljning av medfödda hjärtfel. Modern ekokardiografi tillåter detaljerade kartläggningar av hjärtanatomi, funktion, myokardium, klaffarna och de större kärlen. Transesofageal ekokardiografi (TEE) ger överlägsen bild, jämfört med transthorakal ekokardiografi (TTE), även om sistnämnda är den mest använda metoden.
Ekokardiografi möjliggör även utvärdering av tryck- och volymsbelastning samt upptäckt av hypertrofi och shuntar. Ekokardiografisk bedömning av GUCH-patienter görs av specialiserade undersökare.
Andra viktiga undersökningsmodaliteter är MR hjärta, CT hjärta, ergospirometri (arbetsprov med gasutbytesanalys) och hjärtkateterisering.
Behandlingsprinciper
Större hjärtfel behöver ofta åtgärdas med intervention (kirurgisk eller kateterburen). Utöver interventioner mot själva missbildningen så utvecklar dessa patienter ofta komplikationer som behöver behandlas. Bland dessa komplikationer återfinns exempelvis hjärtsvikt, ventrikulära arytmier (t ex ventrikeltakykardi), supraventrikulära arytmier (t ex förmaksflimmer), pulmonell hypertension, arteriell hypertension (hypertoni), tromboembolism och endokardit. Behandling av dessa komplikationer följer de behandlingsprinciper som används för övriga patientgrupper. Detta är i hög grad en konsekvens av avsaknad av specifika studier i GUCH-populationen. Således är en signifikant del av omhändertagandet baserat på extrapolering av studier genomförda i andra patientpopulationer.
Hjärtsvikt är ett vanligt bland personer med GUCH och behandlingsprinciperna följer de som gäller för vuxna med hjärtsvikt med reducerad ejektionsfraktion (HFREF). Tyvärr baseras dessa rekommendationer på extrapolering av studier som gjorts i andra hjärtsviktspopulationer.
Arytmier är mycket vanliga bland personer med medfödda hjärtfel, även om defekterna åtgärdats med interventioner. Eftersom individer med GUCH ofta har reducerad hjärtfunktion så kan även lindrigare arytmier föranleda hemodynamisk påverkan och dekompensation.
Patienter med GUCH som drabbats av plötslig synkope bör observeras noggrant eftersom dessa har ökad risk för hjärtstillestånd och plötslig död. De missbildningar med störst risk är Fallots tetralogi, transposition av de stora kärlen (TGA, transposition of the great arteries), CCTGA (Congenitally corrected transposition of the great arteries), aortastenos och enkammarhjärta (UVH, univentricular heart).
Förmaksseptumdefekt (ASD, Atrial Septal Defect)
Vid ASD flödar blod från vänster förmak till höger förmak. Flödet från vänster till höger förklaras av att trycket är högre på vänster sida och då utjämnas trycket genom att blod flödar till höger förmak. Detta leder till volymsbelastning på höger sida och konsekvensen av detta är dilatation av höger förmak och höger kammare.
Vid ASD shuntas blod från vänster förmak till höger förmak. Tillstånd som leder till höga tryck på vänster sida (hypertoni, kardiomyopati, aortainsufficiens, aortastenos, mitralisinsufficiens, mitralisstenos) kan leda till ökad shuntning från vänster till höger.
Vid förmaksseptumdefekt stiger därför trycket i höger kammare, vilket leder till att ventrikelseptum buktar in i vänster kammare. Detta ger vänster kammare ett D-format utseende i PSAX (parasternal kortaxelvy). Pga volymsbelastning så ökar höger kammares slagvolymer, vilket leder till ökad genomblödning av lungkärlen. Med tiden tenderar PVR (pulmonell vaskulär resistans; lungkärlresistens) och PA-trycket stiga. stegringen i PVR och PA-tryck kan leda till att trycket på höger sida successivt överstiger trycket på vänstersida, varvid blod shuntas från höger förmak till vänster förmak och då blir patienten cyanotisk. Detta tillstånd kallas Eisenmengers syndrom.
Estimering av shuntstorlek
Man estimerar shuntens storlek genom att skatta blodflödet genom lungorna och blodflödet genom systemcirkulationen, vilket kan görs genom att jämföra höger och vänster kammares slagvolymer. Höger kammares slagvolym beräknas med pulsad doppler i truncus pulmonalis eller RVOT. Vänster kammares slagvolym beräknas med pulsad doppler i LVOT.
Slagvolym (SV) vänster kammare:
SVLVOT = AreaLVOT · VTILVOT
Slagvolym (SV) höger kammare:
SVRVOT = AreaRVOT · VTIRVOT
Shuntstorleken beräknas med följande formel:
SVRVOT/SVLVOT
Om slagvolymen är 120 ml respektive 40 ml blir shuntstorleken:
120/40 = 3
Detta skrivs som 3:1 shunt (”3 till 1 shunt”). Denna beräkning blir osäker vid pulmonalisinsufficiens och aortainsufficiens, eftersom dessa klaffvitier försvårar beräkning av slagvolym.
Typer av förmaksseptumdefekt (ASD)
Förmaksseptumdefekt (ASD) är, näst efter bikuspid aortaklaff, den vanligaste medfödda hjärtmissbildningen. Förmaksseptumdefekter indelas i fölajnde fyra typer:
- Sekundum (Sekundumdefekt)
- Primum (Primumdefekt)
- Sinus venosus (Sinus venosus-defekt)
- Sinus coronarius (Sinus coronarius-defekt)
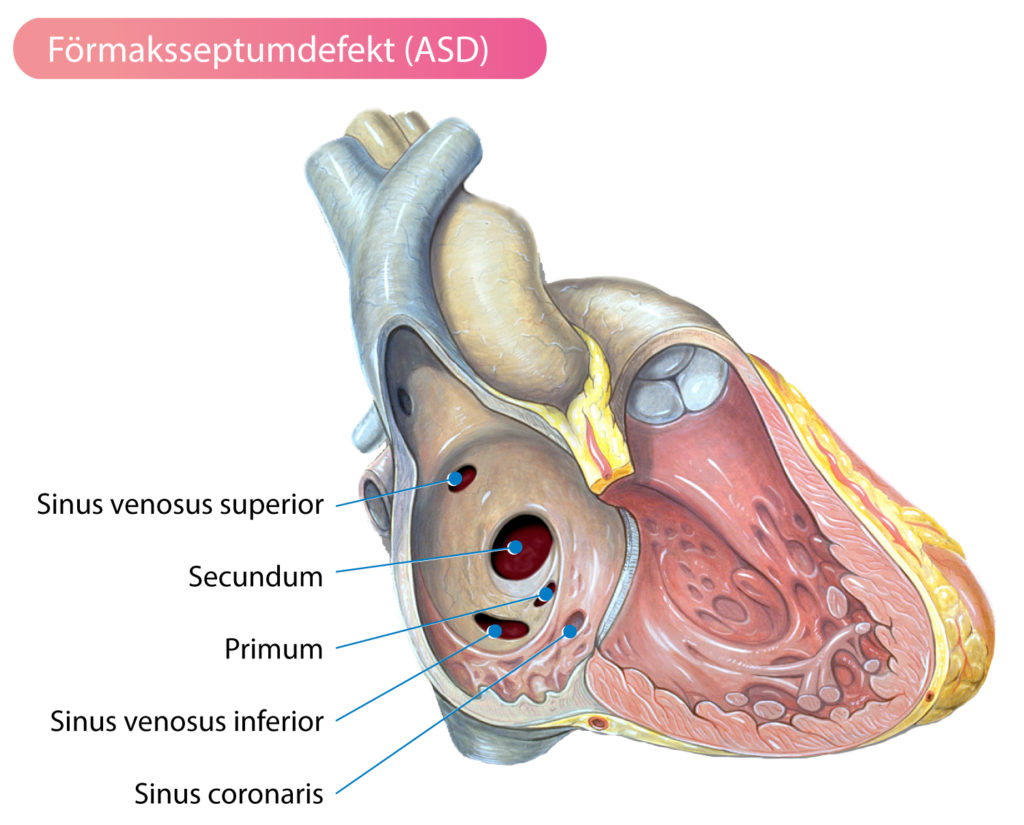
Cirka 80% av alla förmaksseptumdefekter utgörs av sekundumdefekter och dessa är belägna i fossa ovalis med omnejd. Sekundumdefekter inkluderar defekter i foramen ovale. Multipla sekundumdefekter förekommer. Transthorakal ekokardiografi (TTE) kan visualisera större defekter men transesofageal ekokardiografi (TEE) krävs för säker diagnostik.
Primumdefekter (15% av alla ASD) är belägna långt ner i förmaksseptum, vid AV-planet. Primumdefekter är ofta ackompanjerade av defekter i mitralisklaffen eller trikuspidalisklaffen (den vanligaste defekten är ett kluvet främre mitralissegel, vilket kan leda till mitralisinsufficiens. Primumdefekter ses bäst med TEE men kan ofta ses med TTE.
Sinus venosus-defekter drabbar vena cava superior (5%) eller inferior (<1%). Dessa defekter kan leda till att lungvenerna töms i höger förmak eller i vena cava superior/inferior. TEE behövs för att upptäcka dessa defekter.
Sinus coronarius-defekt (<1%) är ovanligt och sitter i sinus coronarius mynning till höger förmak. I dessa fall saknar sinus coronarius tak (”unroofed coronary sinus”), vilket gör att förmaken sammankopplas.
ASD är som regel asymptomatiskt fram till vuxen ålder. Efter 40 års ålder tenderar patienterna utveckla tecken till högersidig hjärtsvikt. Supraventrikulära arytmier (förmaksflimmer, förmaksfladder) är vanligt. Allvarlig pulmonell hypertension drabbar <5%. Paradoxala embolier förekommer men är sannolikt ovanligare än embolier som härrör från förmaksöronen under episoder med förmaksflimmer.
Högerkammarbelastning (volymbelastning) är kardinalfyndet vid ekokardiografi.
Ventrikelseptumdefekt (VSD)
Defekter i ventrikelseptum är vanliga och kan upptäckas när som helst under livet. Ju större defekterna är och desto större hemodynamisk påverkan, desto tidigare upptäcks de. De flesta defekter upptäcks under barndomen eller ungdomsåren. Defekter som upptäcks i vuxen ålder är små och saknar oftast hemodynamisk betydelse. De flesta VSD som upptäcks under spädbarnsåren sluts spontant under det första levnadsåret.
Ventrikelseptum defekt kan förekomma isolerat eller kombinerat med mer komplexa hjärtfel (t ex Fallots tetralogi, transposition av de stora kärlen).
VSD leder till volymsbelastning på vänster kammare, trots att blodet shuntas till höger kammare. Man tror att detta beror på att höger kammare mottager shuntat blod under systole och lyckas transportera det direkt till lungorna och vidare till vänster förmak och kammare som blir belastade. VSD leder därför till dilatation och belastning på vänster kammare. Liksom vid ASD ökar perfusionen genom lungorna, vilket kan leda till pulmonell hypertension. Med kontinuerlig doppler kan flödet över en VSD användas för att beräkna tryckgradient mellan rummen.
Baserat på defektens position i ventrikelseptum indelas VSD i följande varianter:
- Membranös VSD: vanligast (80%) och drabbar membranösa delen av ventrikelseptum. Dessa defekter ses bäst i parasternala snitt. I SAX lokaliserad klockan 10. Spontan slutning är vanligt. Vid spontan slutning kan ett aneurysm uppstå. Aortaklaffens stöd försämras, med risk för aortainsufficiens.
- Muskulär VSD (15%): Kan finnas var som helst i septums muskulösa del. Kan förekomma multipla samtidigt. Spontan slutning särskilt vanligt. Kan ses i apikal fyrkammarvy (A4C) och kortaxelvy (SAX).
- Utflödes-VSD(5%): ses i SAX och är lokaliserad klockan 2, nedom vä aortacuspen och pulmonalisklaffen. Aortaklaffens stöd försämras, med risk för aortainsufficiens. Spontan slutning mindre vanligt.
- Inflödes-VSD (<1%): Lokaliserad i inflödesdelen av septum. Typiskt vid Downs syndrom. Ofta stora. Ses i 4C. Spontan slutning mindre vanligt.




Gerbode-defekt
Eftersom trikuspidalisklaffen är mer apikalt beläget än mitralisklaffen så kan en VSD leda till att blod shuntas från vänster kammare upp till höger förmak, enligt nedanstående figur. Denna typ av defekt kallas Gerbode-defekt.

Peristerande ductus arteriosus (PDA)
Ductus arteriosus är fosterlivets förbindelse mellan pulmonalisartären och aorta descendens. PDA är sällsynt i vuxen ålder. Defekten leder till volymbelastning på vänster kammare och risk för pulmonell hypertension. PDA ses bäst med färgdoppler i suprasternal vy eller kortaxelvy (SAX). Bilden fokusera på truncus pulmonalis och bifurkationen. Flödet i förbindelsen går från aorta till pulmonalis under hela hjärtcykeln.

Coarctatio aortae (CA)
Coarctatio aortae innebär att det finns en förträngning längs aorta och denna förträngningen är oftast belägen i aorta descendens, varför den kan ses från suprasternal vy. Färgdoppler visar turbulent flöde och kontinuerlig doppler visar ökade hastigheter.

Ebsteins anomali
Normalt är trikuspidalisklaffen mer apikalt belägen än mitralisklaffen. Epsteins anomali innebär att trikuspidalisklaffens apikala förskjutning är mycket uttalad. Kriteriet för Epsteins anomali är att trikuspidalisklaffplanet är beläget >10 mm apikalt om mitralisklaffplanet. Trikuspidalisklaffen kan förskjutas ända ner i höger kammares apex och som regel föreligger en mer eller mindre uttalad trikuspidalisinsufficiens.

Kongenitalt korrigerad transposition av de stora kärlen
Transposition av de stora kärlen (TGA, Transposition of the Great Arteries) innebär att två eller flera av de stora kärlen bytt plats. Oftast har aorta och pulmonalisartären bytt plats vilket leder till att vänster kammare pumpar blod till lungorna och höger kammare pumpar blod till systemcirkulationen. Blodet på vänster sida cirkulerar mellan lungorna och vänster hjärthalva. Blodet på höger sida cirkulerar mellan systemcirkulationen och höger hjärthalva. Det betyder att blodet som flödar genom systemcirkulationen inte är syrsatt, vilket leder till dödlig hypoxi. Enda chansen till överlevnad är om det finns en shunt som medger shuntning av blod mellan cirkulationerna. Öppetstående ductus arteriosus, ASD och VSD är i dessa fall livräddande. Idag upptäcks dessa missbildningar fort och de kan åtgärdas kirurgiskt.
Korrigering av transposition innebär att man kopplar om de stora kärlen så att de leder blod från rätt kammare. Höger kammare kommer då fungera som vänster kammare och vice versa.

