Ny föreslagen klassificering av akuta hjärtinfarkt: ocklusionsinfarkt (OMI) och icke-ocklusionsinfarkt (NOMI)
Araz Rawshani, MD, PhD
Specialistläkare, Kardiologi, Sahlgrenska Universitetssjukhuset
Docent, Institutionen för Medicin, Göteborgs Universitet
Den traditionella klassificeringen av akuta koronara syndrom (AKS) i ST-höjningsinfarkt (STEMI), icke-ST-höjningsinfarkt (NSTEMI) och instabil angina (eng. unstable angina, UA) har präglat kliniska riktlinjer i närmare två decennier. Denna klassificering har dock begränsningar, vilket delvis förklaras av metodens fokus på ST-höjningar samt kriterierna för diagnostiska ST-höjningar. Flera studier indikerar att en betydande andel av patienter med en akut ocklusion i ett kranskärl, vilket skall behandlas med omedelbar reperfusion, missas av dessa kriterier. Successivt har en ny klassificering föreslagits: ocklusionsmyokardinfarkt (Occlusion Myocardial Infarction, OMI) och icke-ocklusionsmyokardinfarkt (Non-Occlusion Myocardial Infarction, NOMI). Det föreslagna konceptet lägger större tonvikt på den kliniska kontexten, avancerad EKG-tolkning, ekokardiografi och ett särskilt beaktande av höga troponinnivåer (Ricci et al).
OMI definieras som akut ocklusion i ett kranskärl, vilket orsakar omfattande ischemi och kräver omedelbar reperfusionsbehandling, oaktat EKG-förändringar. Flera studier har visat att OMI-kriterier, vilka inkluderar subtila och icke-traditionella EKG-mönster såsom de Winters T-vågor, Wellens syndrom, m fl, har högre känslighet än traditionella STEMI-kriterier. Upp till 30% av patienter som initialt klassificeras som NSTEMI har en OMI, vilket bör behandlas med akut reperfusion. Dessa patienter har infarktstorlek och dödlighet jämförbar med STEMI-patienter, men erhåller dessvärre fördröjd reperfusion (Sankardas et al).
Flera av de rekommendationer som föreslås inom OMI/NOMI-konceptet återfinns redan i befintliga riktlinjer, men oftast i form av sidospår eller fotnoter snarare än centrala behandlingsprinciper. Ett exempel är djupa, symmetriska T-vågsinverteringar vid bröstsmärta (en välkänd markör för proximal LAD-ocklusion) som i nuvarande riktlinjer inte betraktas som en tydlig indikation för omedelbar reperfusionsbehandling. OMI/NOMI-konceptet syftar till att systematiskt samla ett bredare spektrum av tecken på akut kranskärlsocklusion (OMI) och att lyfta fram dessa som tydliga indikationer för akut reperfusion. Huruvida detta koncept kommer att införlivas i svenska och europeiska riktlinjer återstår att se. Även om så inte sker, är det av klinisk betydelse att känna till vilka patienter som faller inom OMI-gruppen, för att dessa ska kunna identifieras i tid och få ett mer adekvat omhändertagande.
Akuta koronara syndrom
Den befintliga klassificeringen av akuta koronara syndrom (AKS) i ST-höjningsinfarkt (STEMI), icke-ST-höjningsinfarkt (NSTEMI) och instabil angina (UA) har under lång tid legat till grund för diagnostik och behandling. Dock har denna klassificering begränsningar, framför allt dess fokus på ST-höjning som den primära signalen för att genomföra akut koronarangiografi och PCI. Denna metod misslyckas med att identifiera en betydande andel patienter med akut koronartrombos (ACO) som inte uppfyller de etablerade EKG-kriterierna för STEMI, vilket leder till förseningar i potentiellt livräddande behandlingar. Denna begränsning har uppmärksammats i samtida kliniska riktlinjer (Byrne et al, 2023).
OMI/NOMI syftar till att basera terapeutiska beslut på risken för akut ocklusion (OMI), snarare än på strikta EKG-kriterier. De senaste åren har flera maskininlärningsmodeller för EKG-tolkning utvecklats i syfte att skilja mellan OMI och NOMI, vilket speglar det växande behovet av en mer träffsäker diagnostik av akuta ocklusioner (Al-Zaiti et al, 2023).
Den föreslagna övergången från STEMI/NSTEMI/UA till OMI/NOMI stöds av observationsstudier och klinisk erfarenhet. Studier har visat att en betydande andel av patienterna med akut koronartrombos inte uppvisar klassisk ST-höjning på EKG, vilket leder till uttalade förseningar i reperfusionsbehandling. Avancerad EKG-tolkning, i kombination med klinisk bedömning och bilddiagnostik, har visat sig förbättra identifieringen av dessa patienter. Trots att nuvarande riktlinjer fortsatt bygger på den traditionella klassificeringen, har OMI/NOMI-ansatsen vunnit gehör bland kliniker (Ricci et al).
Mekanismer bakom akuta koronara syndrom
Akuta koronara syndrom utgör ett spektrum av kliniska tillstånd som sträcker sig från instabil angina till hjärtinfarkt, och orsakas av en plötslig obstruktion av blodflödet i kranskärlen. Flera distinkta patologiska mekanismer kan leda till AKS (Kraler et al, 2025):
Plackruptur
Plackruptur är den vanligaste bakomliggande mekanismen vid AKS. Det inträffar när en tunn fibrös kapsel ovanpå en lipidrik ateromatös kärna brister, vilket exponerar det starkt trombogena kärninnehållet för blodbanan. Denna exponering utlöser aktivering och aggregation av trombocyter samt koagulationskaskaden, vilket leder till bildning av tromb som delvis eller fullständigt kan täppa till det drabbade kranskärlet. Plackruptur står för cirka 60% av STEMI-fallen.
Plackerosion
Vid plackerosion skadas plackets endoteliala ytskikt utan att den fibrösa kapseln brister. Denna mekanism är vanligare hos yngre individer, rökare och kvinnor. Det exponerade subendoteliala matrixet främjar trombocytadhesion och trombbildning. Plackerosion beräknas bidra till cirka 25–44 % av alla AKS-fall och tenderar att vara associerat med mindre lipidrika plack jämfört med plackruptur.
Kalcifierade noduli
Kalcifierade noduli svarar för omkring 5% av alla AKS. Dessa uppkommer när täta, kalciumavlagringar i placket stör den fibrösa kapseln och skjuter ut i kärllumen. Dessa utsprång kan orsaka mekanisk skada på endotelet och främja lokal trombosbildning.
Koronar vasospasm
Koronar vasospasm innebär en övergående spasm i ett epikardiellt kranskärl, vilket reducerar eller helt stoppar blodflödet. Denna mekanism kan orsaka ischemi eller infarkt även i frånvaro av signifikant aterosklerotiskt plack. Vasospasm kan uppträda spontant eller utlösas av faktorer som stress, kyla, vissa läkemedel eller rökning. Det är en vanlig mekanism bakom variantangina (Prinzmetals angina).
Koronaremboli
Embolier kan hamna i kranskärlen och obstruera blodflödet. Embolikällan kan vara tromber i vänster förmak (t.ex. vid förmaksflimmer), endokarditvegetationer eller paradoxala embolier via ett öppet foramen ovale.
Spontan koronarartärdissektion (SCAD)
Spontan dissektion av kranskärl kännetecknas av en spontan bristning i kärlväggen, vilket skapar ett falskt lumen mellan intiman och median, eller mellan median och adventitian. Blod som tränger in i detta falska lumen komprimerar den äkta lumenet, vilket obstruerar distalt blodflöde. SCAD är vanligare hos unga till medelålders kvinnor och är ofta associerad med fibromuskulär dysplasi, graviditetsrelaterade tillstånd eller extrem stress.
Oavsett bakomliggande mekanism påverkas det kliniska förloppet av flera faktorer: ocklusionens läge (proximalt eller distalt), närvaro av kollateralcirkulation, ocklusionens duration samt trombosens dynamik (bildning och upplösning av trombmassa). Dessa faktorer påverkar utsträckningen och intensiteten av myokardischemi och därmed symptomatologin, hemodynamisk stabilitet och EKG-förändringar. Till exempel kan en proximal ocklusion med god kollateralcirkulation resultera i få EKG-förändringar och milda symptom, medan en proximal ocklusion utan kollateraler kan orsaka plötsligt hjärtstopp.
Ett nytt sätt att klassificera akuta koronara syndrom
Den traditionella klassificeringen av akuta koronara syndrom i STEMI, NSTEMI och instabil angina (UA) baseras på EKG-fynd samt förekomst av hjärtskademarkörer (troponin). I riktlinjer och forskningssammanhang används dessutom den förenklade klassificeringen STE-AKS / NSTE-AKS. STE-AKS (ST-Elevation AKS) är i princip synonymt med STEMI, medan NSTE-AKS (icke-ST-Elevation AKS) inbegriper både NSTEMI och instabil angina. Principen för indelningen är att patienter med STE-AKS har som regel drabbats av en akut ocklusion som kräver omedelbar angiografi och PCI. Patienter med NSTE-AKS har oftast inte drabbats av en totalocklusion och prognosen, för hela gruppen, påverkas inte av akut angiografi och PCI. Dock visar flera studier att denna metod missar en betydande andel patienter med akut kranskärlsocklusion, vilket förklaras av att ST-höjning är en ofullständig markör för ocklusion. Ungefär 30% av akuta ocklusioner förbises om man enbart förlitar sig på standardkriterier för STEMI, vilket leder till fördröjd reperfusion och sämre kliniska utfall (Ricci et al). Samtidigt är specificiteten för ST-höjningar inte fullständigt, vilket förklaras av att det finns många orsaker till ST-höjningar och bröstsmärta är ett vanligt symtom.
Det föreslagna konceptet ocklusionsmyokardinfarkt (Occlusion Myocardial Infarction, OMI) fokuserar på att identifiera ocklusioner genom avancerad EKG-tolkning och beaktande av specifika kliniska karaktäristika för ocklusioner utan ST-höjningar. Forskning visar att OMI/NOMI-konceptet förbättrar den diagnostiska sensitiviteten (78% jämfört med 44%; Ayyad et al). Identifiering av akuta ocklusioner i frånvaro av ST-höjningar möjliggör tidigare intervention, vilket potentiellt förbättrar prognosen för högriskpatienter som annars skulle erhålla subakut (fördröjd) angiografi.
En central aspekt i detta sammanhang är den snabba utvecklingen av artificiell intelligens (AI). Särskilt djupinlärning (eng. deep learning) har visat sig vara ett mycket kraftfullt verktyg för att utveckla multimodala prediktionsmodeller, det vill säga datormodeller som kan integrera information från flera olika källor, såsom EKG-signaler, anamnes och blodprover, för att med hög precision bedöma risken för hjärtinfarkt och kranskärlsocklusion (Hilgendorf et al). Sådana prediktionsmodeller kommer sannolikt bli det dominerande verktyget för bedömning av patienter med misstänkt AKS.
Även om OMI/NOMI-konceptet förefaller ha flera fördelar och flera studier visar lovande resultat, så krävs randomiserade kliniska prövningar för att validera att metoden är överlägsen den befintliga rutinen.
Nuvarande klassificering av AKS
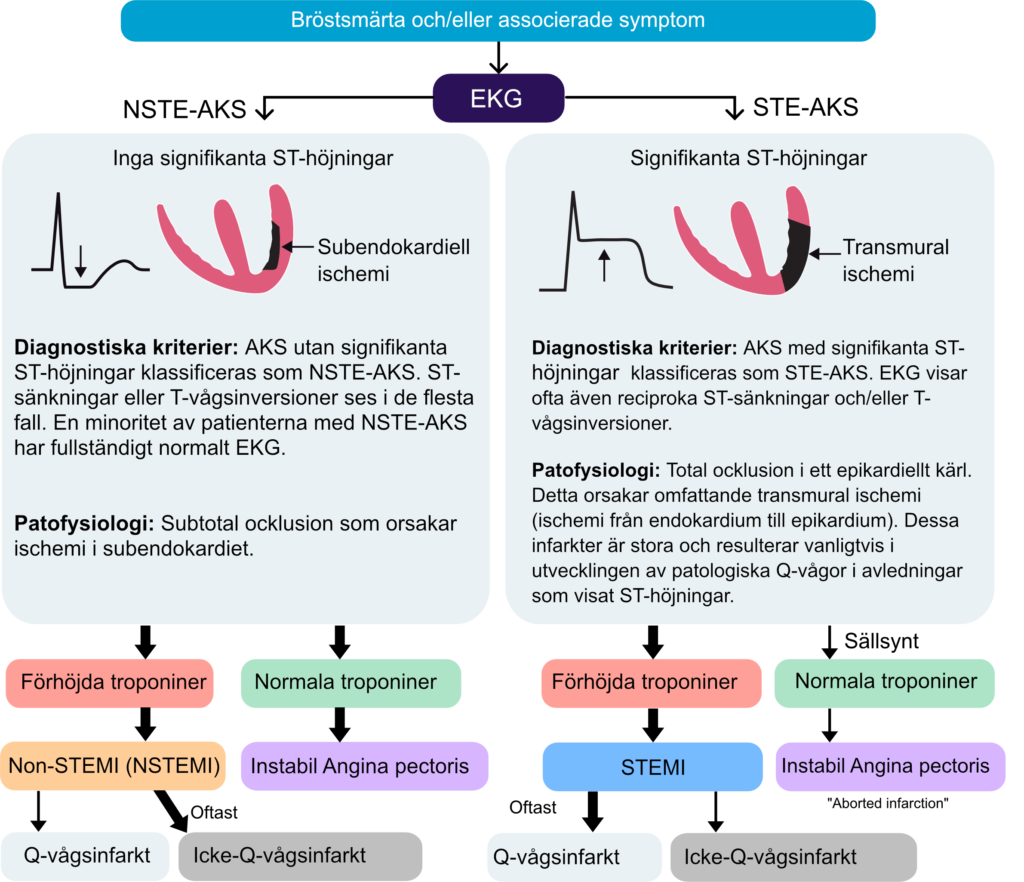
Instabil angina (UA)
Instabil angina definieras som myokardischemi i vila eller vid minimal ansträngning, utan tecken på myokardnekros. Det orsakas oftast av minskat koronarblodflöde till följd av en mycket tät stenos eller en partiell tromb. Kliniskt kan instabil angina yttra sig som nytillkommen, försämrad eller viloangina som är långvarig och inte lindras av adekvat av nitroglycerin. EKG kan visa ST-sänkning, inverterade T-vågor, eller vara helt normalt.
NSTEMI (icke-ST-höjningsinfarkt)
NSTEMI definieras som myokardnekros orsakad av akut ischemi, vilket bekräftas genom förhöjda hjärtskademarkörer (troponin). Det orsakas typiskt av en partiell eller övergående ocklusion av ett kranskärl och leder till subendokardiell infarkt. Symtomen liknar de vid instabil angina men är mer uttalade. Diagnosen baseras på klinisk presentation, EKG (ST-sänkningar, T-vågsinversioner) och förhöjda troponinnivåer. De flesta patienter genomgår angiografi inom 24–72 timmar, med snabbare intervention för patienter med mycket hög risk. Patienter med övergående ST-höjningar (dvs. <20 minuter) klassificeras också som NSTEMI.
STEMI (ST-höjningsinfarkt)
STEMI diagnostiseras på basen av ischemiska symtom och ihållande ST-höjning (dvs. >20 minuter) i två eller fler angränsande avledningar: ≥1 mm i samtliga avledningar utom V2–V3, där tröskelvärdena är ≥2 mm hos män ≥40 år, ≥2,5 mm hos män <40 år, och ≥1,5 mm hos kvinnor. Dessa fynd utgör den huvudsakliga grunden för att initiera akut koronarangiografi och reperfusionsbehandling.
STEMI-negativ ocklusionsinfarkt
Begreppet STEMI-negativ ocklusionsmyokardinfarkt (STEMI-negativ OMI) avser den grupp som saknar diagnostisk ST-höjning på EKG, men som har ett akut ockluderat kranskärl. Flera studier och metaanalyser visar att cirka 25–30 % av de patienter som initialt klassificeras som NSTEMI i själva verket har en akut kranskärlsocklusion. Vissa studier rapporterar att denna andel kan vara så hög som 47% i vissa NSTEMI-populationer som genomgår angiografi (Ricci et al). Herman et al visade att konventionella STEMI/NSTEMI-kriterier misslyckas att diagnostisera 67% av fallen med ocklusionsinfarkt. Dessa förbisedda fall, benämnda STEMI-negativ OMI, utgör ett betydande kliniskt problem. Bland de STEMI-negativa OMI-patienter som undersöktes av Herman et al erhöll endast 34% revaskularisering inom två timmar.
Förmåga att tolka EKG vid AKS
Läkares och sjuksköterskor förmåga att diagnostisera STEMI har undersökts i en lång rad studier. Exempelvis visade McCabe et al följande beträffande läkares förmåga att diagnostisera STEMI:
- Sensitiviteten för att korrekt diagnostisera STEMI var 65%.
- Specificiteten för att korrekt utesluta STEMI var 79%.
- Fem år klinisk erfarenhet adderade 6% högre sannolikhet för korrekt tolkning.
- Efter justering för erfarenhet fanns inga signifikanta skillnader i diagnostisk precision mellan akutläkare, kardiologer och interventionskardiologer.
Begränsningar med 12-avlednings-EKG
Ett 12-avlednings-EKG är tveklöst en mycket användbar metod för att diagnostisera akuta koronara syndrom, men metoden har flera tillkortakommanden. Först och främst är specificiteten (avseende ST-höjningar, ST-sänkningar och T-vågsförändringar) låg eftersom sådana förändringar är vanliga på EKG hos friska samt hos personer med andra tillstånd. Sedermera är sensitiviteten låg i flera situationer, särskilt följande:
- Infarkt som drabbar vänster kammares bakre vägg (posterior infarkt).
- Infarkt som drabbar höger kammare.
- Infarkter orsakade av ocklusion i vänster cirkumflexartär (LCX).
Därutöver kan patienter med OMI uppvisa subtila ST-höjningar som inte uppfyller formella kriterier för STEMI. Förloppet vid akuta koronara syndrom är högst dynamiskt och patienter med ett helt normalt EKG vid ankomst kan inom loppet av några minuter utveckla dramatiska ST-höjningar; därför bör man inte förlita sig kompromisslöst på millivoltbaserade kriterier.
- Marti et al undersökte 504 patienter med misstänkt STEMI som genomgick primär PCI. Av dessa hade 20% endast subtil ST-höjning (0.1–1.0 mm), vilket ändå visade sig indikera akut koronartrombos.
- Aslanger et al studerade fall av OMI som initialt missats enligt STEMI-kriterier. De fann att tre fjärdedelar av dessa kunde identifieras genom subtila eller dynamiska ST-förändringar.
- Meyers et al studerade 146 patienter som diagnostiserats med hjälp av OMI-specifika EKG-kriterier i stället för konventionella STEMI-kriterier. Detta möjliggjorde tidigare upptäckt av fler akuta ocklusioner.
- Khan et al genomförde en metaanalys av över 40 000 NSTEMI-patienter och fann att cirka 25% hade ett helt ockluderat kärl vid angiografi, oftast i höger kranskärl eller vänster cirkumflexa. Dessa patienter hade signifikant högre frekvens av allvarliga kardiovaskulära händelser (MACE) samt totalmortalitet jämfört med NSTEMI-patienter utan total ocklusion.
STEMI-ekvivalenter
Begreppet STEMI-ekvivalenter utgör ett försök att bredda de diagnostiska kriterierna och inkludera fler EKG-mönster som tyder på OMI. Dessa ekvivalenter är viktiga, men de erbjuder inte ett heltäckande ramverk för att vägleda reperfusionsstrategier. OMI/NOMI-modellen utgör ett mer komplett alternativ, där behandling styrs av ett helhetsperspektiv med fokus på akuta ocklusioner.
Ocklusionsinfarkt (OMI) vs. icke-ocklusionsinfarkt (NOMI)
Ocklusionsmyokardinfarkt (OMI)
Ocklusionsmyokardinfarkt (OMI) definieras som en akut hjärtinfarkt till följd av en akut total eller nära-total ocklusion i ett kranskärl, där kollateralcirkulationen är otillräcklig för att förhindra transmural ischemi och infarkt. Omedelbar reperfusion krävs för att begränsa infarktstorlek och minska risken för maligna ventrikulära arytmier.
OMI är en patofysiologisk och klinisk diagnos som integrerar följande parametrar:
- Klinisk presentation (t.ex. typisk ischemisk bröstsmärta, hemodynamisk instabilitet, arytmier)
- Avancerad EKG-tolkning (inklusive subtila fynd, utöver klassisk ST-höjning)
- Hjärtskademarkörer
- Ekokardiografi
Angiografiska fynd som talar för ocklusion (t.ex. TIMI-flöde grad 0, 1 eller 2) utgör ett viktigt indicium. Även TIMI 3-flöde kan vara förenligt med en nyligen reperfunderad OMI om det föreligger mycket höga troponinnivåer, vilket indikerar att en uttalad ischemi förelegat innan reperfusionen.
Icke-ocklusionsmyokardinfarkt (NOMI)
NOMI omfattar följande infarkter:
- Infarkter som inte orsakats av en akut, persisterande ocklusion i kranskärlet, eller
- Infarkter som inträffat i ett kärl med tillräcklig kollateral cirkulation för att förhindra transmural ischemi.
Den bakomliggande mekanismen kan vara som följer:
- Infarkt till följd av plackruptur med icke-ocklusiv tromb.
- Fall med spontan reperfusion (via endogen trombolys) innan ST-lyft eller andra tecken på OMI uppkommit.
- MINOCA (myokardinfarkt i icke-obstruktiva kranskärl), t.ex. på grund av spasm, mikrovaskulär dysfunktion eller embolism.
- Typ 2-infarkt orsakad av supply-demand-obalans (t.ex. vid anemi, takykardi i närvaro av stabil kranskärlssjukdom).
Patienter med NOMI har inte nytta av akut reperfusion (dvs. inom <2 timmar). Däremot är tidig koronarangiografi (inom 24–72 timmar) indicerad.
Evidens för OMI/NOMI-metoden
Enstaka studier har jämfört handläggning enligt OMI/NOMI-kriterier med traditionella STE-AKS/NSTE-AKS-kriterier bland patienter med angiografiskt bekräftad akut ocklusion.
Meyers et al. (2021)
Meyers och kollegor visade att avancerad EKG-bedömning med fokus på OMI-tecken, utöver enbart ST-höjningar, hade avsevärt högre sensitivitet för att detektera akut ocklusion. Sensitiviteten var 80–86%, jämfört med 36–41% för traditionella STEMI-kriterier, samtidigt som specificiteten var likvärdig eller bättre.
Studien visade också att:
- STEMI-negativa OMI-patienter hade lika stora infarkter som STEMI-positiva OMI-patienter.
- De fick dock signifikant fördröjd reperfusion.
- OMI-baserad tolkning möjliggjorde diagnos av ACO i median 1,5 timmar tidigare än traditionella kriterier.
DIFOCCULT-studien
Denna kohortstudie (n=3000) undersökte huruvida ett klassificeringssystem baserat på OMI/NOMI var bättre än STE-AKS/NSTE-AKS för att identifiera patienter i behov av akut reperfusion. Studien visade följande:
- 28.2% av fallen som ursprungligen klassificerats som NSTEMI uppvisade EKG-fynd förenliga med akut ocklusion. Dessa patienter hade högre förekomst av ocklusioner, större myokardskada och sämre prognos.
- OMI/NOMI-baserad strategi var bättre på att förutsäga verklig ocklusion och mortalitet än standardmetoden.
Koyama et al
I en prospektiv studie tillämpade Koyama och kollegor en omedelbar invasiv strategi (akut angiografi) för samtliga patienter med misstänkt AKS, även de klassificerade som NSTEMI. Studien visade följande:
- Bland misstänkta NSTEMI-patienter hade 63% begränsat koronarflöde och 47% hade TIMI 0-flöde.
- Trots skillnader i EKG-förändringar var mortaliteten på sjukhus och efter 6 månader jämförbar mellan NSTEMI- och STEMI-grupperna.
Diagnostik av ocklusionsinfarkt (OMI)
Diagnos av OMI kräver ett multimodalt tillvägagångssätt där avancerad EKG-tolkning kombineras med klinisk bedömning, hjärtskademarkörer (troponin) och framgent även AI.
Avancerad EKG-tolkning
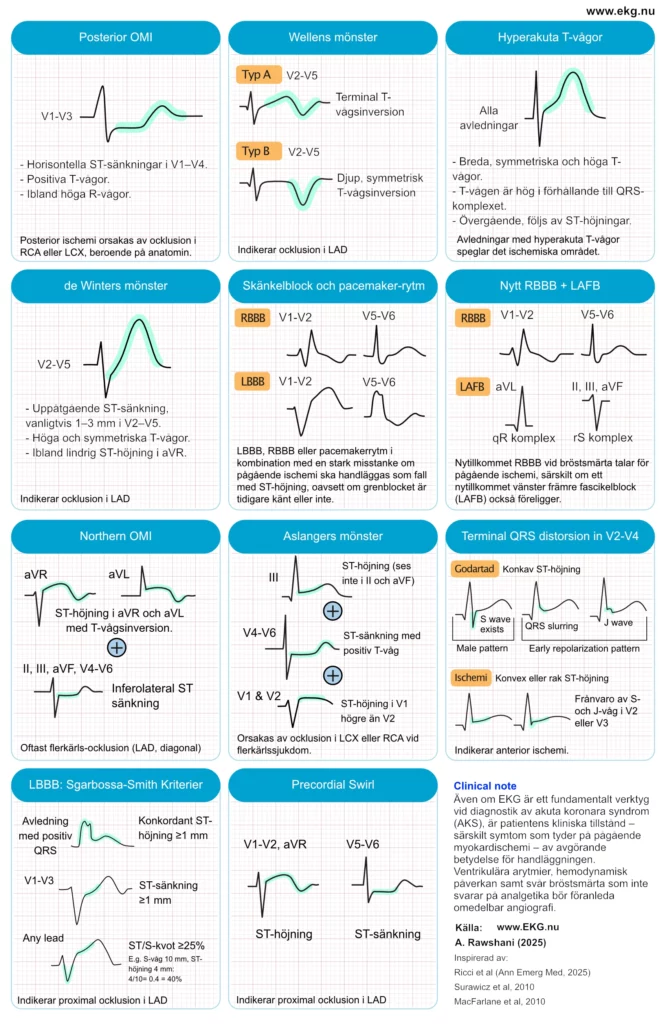
Figur 1. EKG-mönster som antyder OMI.
En hörnsten i OMI/NOMI-strategin är förmågan att känna igen EKG-mönster som tyder på akut ocklusion men som inte uppfyller traditionella STEMI-kriterier. Nedan följer beskrivningar av EKG-mönster som indikerar hög eller mycket hög risk för OMI.
De Winters T-vågor (De Winters tecken)
EKG-fynd
- Uppåtgående ST-sänkning vid J-punkten i V1–V6
- Höga, symmetriska T-vågor i prekordiala avledningar
- Möjlig lätt ST-höjning i aVR
Tyder på akut ocklusion i proximala LAD (vänster främre nedåtstigande artär). Förekommer i ca 2 % av anteriora infarkter. Kräver akut reperfusion trots frånvaro av ST-höjning.
Wellens syndrom (Wellens-mönster)
EKG-fynd
- Biphasiska eller djupt inverterade T-vågor i V2–V3 (kan sträcka sig till V1–V6)
- Minimal eller ingen ST-höjning
- Normala R-vågor, inga patologiska Q-vågor
Indikerar kritisk stenos i proximala LAD. Typiskt sett förekommer detta i smärtfritt tillstånd efter nyligen genomgången angina. Hög risk för stor anterior infarkt om obehandlad.
Posterior hjärtinfarkt
EKG-fynd
- Horisontella ST-sänkningar ≥0,5 mm i V1-V4
- Positiva T-vågor i V1-V4
- Höga R-vågor (R/S-kvot >1 i V2)
- Om posteriora avledningar (V7–V9) används kan ST-höjning i dessa kan bekräfta diagnosen.
Orsakas av ocklusion i vänster cirkumflexa (LCX) eller höger kranskärl (RCA), beroende på vilket kärl som försörjer den posteriora väggen. Posterior infarkt kan uppträda isolerat eller tillsammans med inferior, lateral eller inferolateral infarkt.
Grenblock och pacemakerrytm
Tidigare rekommendationer att behandla ett nytillkommet vänstergrenblock (LBBB) eller nytillkommet högergrenblock (RBBB) som STEMI gäller inte längre. Nuvarande riktlinjer bejakar att förekomsten av LBBB eller RBBB ökar sannolikheten för OMI, och rekommenderar att akut angiografi ska göras vid hög klinisk misstanke, oavsett om LBBB/RBBB är känt eller nytillkommet (Byrne et al). Samma princip gäller för patienter med pacemakerrytm.
Sgarbossa-kriterier och Sgarbossa-Smith-kriterier
Dessa kriterier avser underlätta diagnostik av ischemi vid LBBB. Smiths modifiering av de ursprungliga Sgarbossa-kriterierna (Smith et al) är den mest användbara varianten och baseras på följande kriterier:
- Konkordant ST-höjning ≥1 mm i avledningar med positiv QRS
- Konkordant ST-sänkning ≥1 mm i V1–V3
- Diskordant ST-höjning som är ≥25% av föregående S-våg i avledningar med negativ QRS
Sensitiviteten är generellt låg för alla kriterier som framtagits för diagnostik av akuta ocklusioner vid LBBB.
Nytillkommet högergrenblock (RBBB) och främre fascikelblock (LAFB)
Bifascikulärt block (kombination av RBBB och LAFB) talar starkt för proximal LAD-ocklusion om patienten har bröstsmärta eller andra tecken på ischemi. Båda fasciklarna försörjs av septala grenar från LAD. Detta är associerat med större infarkter, högre risk för AV-block III och ökad mortalitet.
Subtil ST-höjning
EKG-fynd
- ST-höjning som ej uppfyller formella STEMI-kriterier (se tidigare).
- ST-höjningen är oproportionerligt högt jämfört med samma avlednings QRS-amplitud.
- Ofta dynamiska förändringar, med T-vågsförändringar eller reciproka ST-sänkningar
Terminal QRS-distorsion
EKG-fynd
- Avsaknad av både S-våg och J-våg i V2 och/eller V3
- I avledningar med Rs-konfiguration: frånvaro av S-våg
- I avledningar med qR-konfiguration: J-punkt ≥50 % av R-vågens amplitud
Hög specificitet för anterior infarkt med proximal LAD-ocklusion.
Patologiska Q-vågor
Även om patologiska Q-vågor ofta ses som tecken på tidigare genomgången infarkt, kan de utvecklas redan inom 2 timmar och därmed indikera pågående OMI som kräver omedelbar reperfusion.
Aslangers mönster
EKG-fynd
- ST-höjning isolerad till avledning III, utan samtidig höjning i II eller aVF
- ST-sänkning i V4–V6 (men inte i V2), med positiva eller terminalt positiva T-vågor
- ST-höjning i V1 är högre än i V2
Tyder på akut inferior infarkt, ofta till följd av LCX-ocklusion med samtidig flerkärlssjukdom. Associerat med större infarktstorlek och högre mortalitet, jämförbart med STEMI-patienter.
Northern OMI
EKG-fynd
- ST-höjning i aVR och aVL, ofta med negativa T-vågor
- ST-sänkning i inferiora (II, III, aVF) och laterala prekordialavledningar (V4–V6), med positiva eller bifasiska T-vågor
Tyder på ocklusion av vänster huvudstam eller proximala LAD. Ett högriskmönster förenat med omfattande myokardischemi.
Prekordiell virvel (eng. Precordial swirl)
EKG-fynd
- ST-höjning i V1 och/eller aVR
- Reciproka ST-sänkningar i V5 och/eller V6
- Hyperakuta eller oproportionerligt höga T-vågor i V1–V2
- Frånvaro av vänsterkammarhypertrofi eller breda QRS-komplex
Tyder på proximal LAD-ocklusion, ofta före första septalgren. Associerat med septal, anterior och apikal ischemi. Ofta förbisett av traditionella STEMI-kriterier.
Ocklusion av vänster cirkumflexa (LCX)
LCX-ocklusion är särskilt svår att upptäcka med standard 12-avlednings-EKG. Detta beror på att LCX försörjer laterala och bakre väggar av vänster kammare, områden som är suboptimalt reflekterade i konventionella avledningar.
EKG-fynd
- ST-höjning i laterala avledningar (I, aVL, V5–V6) – även subtila förändringar bör beaktas.
- Reciprok ST-sänkning i inferiora avledningar (III och aVF) – talar för lateral ischemi.
- Hög klinisk misstanke: vid svår bröstsmärta och icke-diagnostiskt EKG bör LCX-ocklusion misstänkas.
Klinisk kontext
Diagnosen OMI ställs aldrig isolerat utifrån EKG-fynd – den kliniska kontexten är avgörande. Följande tillstånd ska kraftigt öka misstanken om pågående OMI och indikera omedelbar reperfusionsstrategi:
- Ihållande ischemirelaterade symtom (t.ex. bröstsmärta, dyspné) som inte svarar på initial medicinsk behandling (t.ex. nitrater)
- Hemodynamisk instabilitet (t.ex. hypotension, tecken på chock)
- Maligna ventrikulära arytmier
- Hjärtstopp som uppträder i samband med typiska ischemiska symtom
Hjärtskademarkörer
Hjärtspecifika troponiner (I eller T) är fortsatt gold standard för att bekräfta myokardnekros.
- Mycket höga nivåer av troponin, t.ex. hs-cTnT >1000 ng/L eller hs-cTnI >200 × övre referensgränsen, tyder på en stor infarkt till följd av större kranskärlsocklusion, även om angiografi visar TIMI 3-flöde.
- Detta kan antyda spontan reperfusion av ett tidigare ockluderat kärl eller ocklusion med initialt god kollateralcirkulation som sedermera blivit otillräckligt.
Artificiell intelligens (AI)
I dagsläget har en rad forskare utvecklat AI-algoritmer specifikt för att detektera OMI/NOMI. Al-Zaiti et al utvecklade och validerade en modell baserad på 7313 patienter. Modellen överträffade läkare i både sensitivitet och specificitet. Al-Zaiti et al föreslåg en OMI-Score (poängskala) som visade sig kunna förbättra både ”rule-in” och ”rule-out” diagnostik, och när den kombinerades med bedömning av särskilt utbildad personal på akutmottagningen kunde den korrekt omklassificera ungefär var tredje patient med bröstsmärta. Forskning pågår även i Sverige (Hilgendorf et al).
Sängnära ekokardiografi
Ekokardiografi är ett värdefullt komplement, särskilt vid:
- Icke-diagnostiskt eller tvetydigt EKG
- Misstänkt OMI med instabil patient
Nytillkommen och lokaliserad hypokinesi eller akinesi i ett eller flera segment (sk regionalitet) förstärker misstanken om OMI och kan stödja beslut om akut koronarangiografi.
Koronar-CT-angiografi (CCTA)
De flesta sjukhus i Sverige erbjuder i dagsläget inte akut CCTA på indikationen AKS. På de sjukhus där diagnostiken är tillgänglig används den i följande situationer:
- EKG och troponin är icke-diagnostiska, och
- Patienten är lågrisk eller intermediärrisk.
CCTA är inte primärt diagnostiskt verktyg vid stark klinisk misstanke om AKS och särskilt inte vid misstanke om OMI – där är snabb invasiv angiografi avgörande.
Behandling av OMI
Patienter som identifieras som STEMI-negativ OMI bör betraktas som kandidater för akut reperfusionsbehandling. Målet bör vara att uppnå samma “door-to-balloon”-tider vid perkutan koronarintervention (PCI) eller “door-to-needle”-tider vid fibrinolys som för STEMI-patienter.
Dock noterar redan existerande riktlinjer från AHA, ACC och ESC majoriteten av dessa principer: den nuvarande rekommendationen är att högriskpatienter med NSTEMI eller instabil angina (UA) bör genomgå brådskande angiografi, oavsett EKG-fynd. Således är OMI/NOMI-strategins huvudsakliga bidrag att tillhandahålla en mer explicit diagnostisk modell som betonar en omfattande utvärdering med hjälp av:
- Avancerad EKG-tolkning
- Bilddiagnostik
- Biomarkörer (troponin)
- Klinisk kontext
Det är ännu oklart om internationella och nationella riktlinjer kommer att övergå från den traditionella indelningen i STEMI/NSTEMI till en strategi baserad på OMI/NOMI. Oavsett om en sådan förändring sker eller inte, har OMI/NOMI-konceptet ett utbildningsvärde. Det uppmuntrar till fördjupad förståelse av subtila EKG-förändringar och främjar ett kliniskt tänkande som sträcker sig bortom de klassiska STEMI-kriterierna.

